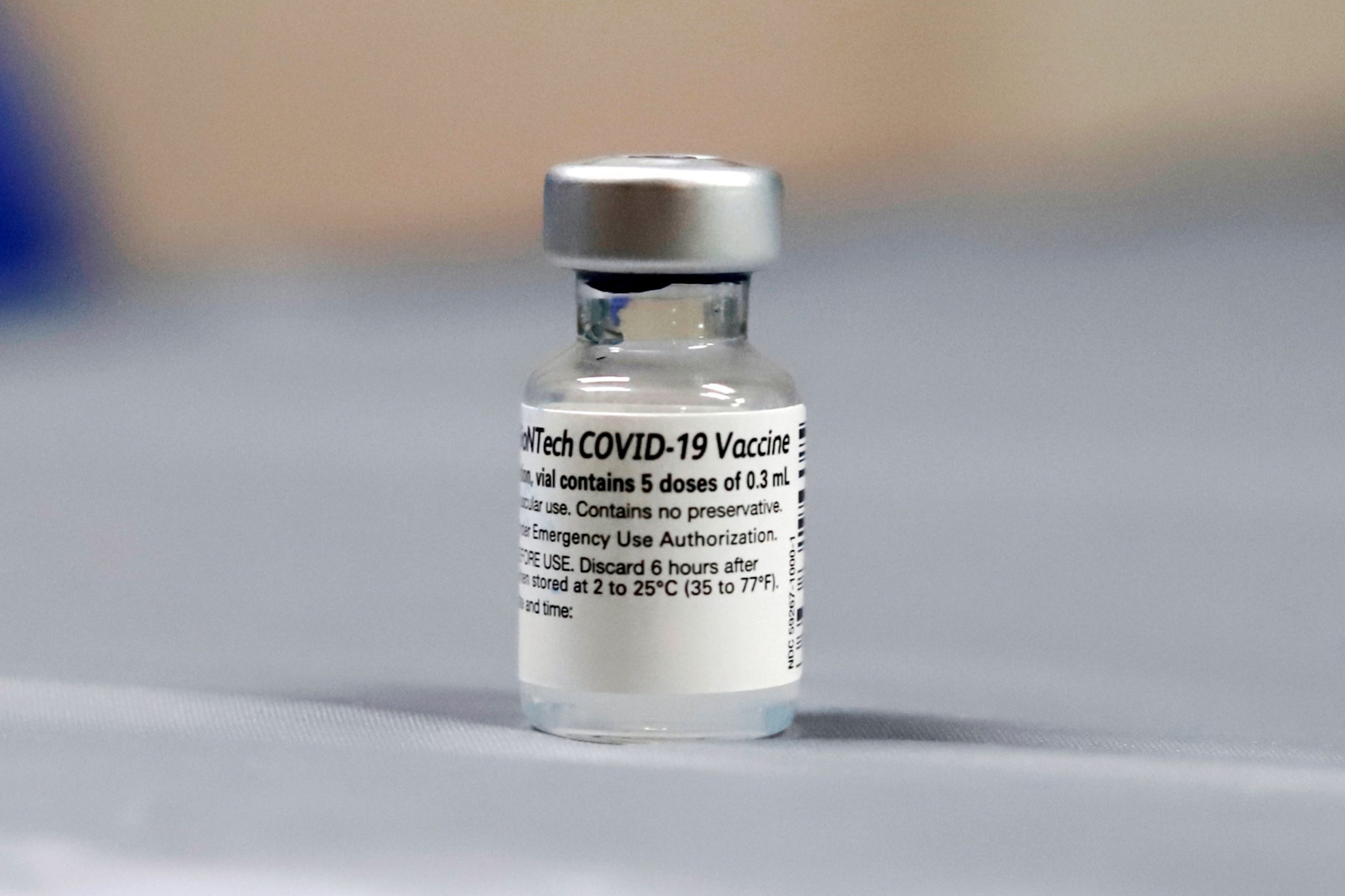
Hasta la fecha se ha hablado mucho sobre las vacunas contra el SARS-CoV2 desarrolladas en países como China, Rusia, Reino Unido o Estados Unidos. Y es que todo el mundo se ha volcado en desarrollar una vacuna que haga frente a esta crisis sanitaria causada por la COVID-19. El objetivo de que haya más de una vacuna desarrollada, o en desarrollo como es el caso de España, es garantizar una protección inmunitaria a millones de personas en todo el planeta.
¿Conoces las vacunas que se están desarrollando en España? Aunque España esté en una situación un tanto peliaguda en lo que respecta a la inversión en ciencia, lo cierto es que se hace muy buena ciencia. Por eso, es importante reconocer que numerosos investigadores en España también están en pie de guerra desde el minuto cero. Quédate y averigua que es lo que se está haciendo con respecto al desarrollo de las “vacunas españolas”.
Índice de contenido:
Introducción
Desde el pasado año, cuando comenzó la pandemia, el Consejo Superior de Investigaciones Científicas (CSIC) puso en marcha no uno, sino tres proyectos de vacuna contra la COVID-19. Los tres se encuentran actualmente en fase preclínica, es decir, aquella fase previa donde se comprueba la seguridad de la vacuna en el laboratorio con ayuda de animales de experimentación, así como de algunas técnicas de cultivo celular. De los tres proyectos, dos están cada vez más cerca de la fase clínica y el restante se espera que entre en esta fase hacia finales de verano o principios de otoño.
La fase clínica, o ensayos clínicos, es la que incluye un determinado número de personas, que irán aumentando de forma creciente según la etapa en la que se encuentre la fase (de la I a la IV). En ellos se evalúa la seguridad y la eficacia de la vacuna candidata, así como los posibles efectos adversos. Finalmente, en base a los resultados de los ensayos en fase III y con la correspondiente documentación, las agencias reguladoras (FDA, EMA, etc.) aprobarán su uso y las vacunas serán comercializadas a toda la población. En este punto, las vacunas (y cualquier medicamento) seguirá siendo evaluada en una fase de farmacovigilancia o fase IV.
En el presente post, nos centraremos en las tres vacunas que se están investigando en el CSIC. Cabe resaltar que esta entidad no sólo se ha dedicado al desarrollo de vacunas, también lo ha hecho de medicamentos que ayuden a paliar o a hacer frente a la enfermedad una vez se produce, así como al desarrollo de nuevos test diagnósticos.
Pero también existen otros seis proyectos más que han llegado recientemente a fase preclínica y que proceden de universidades, hospitales, empresas privadas y otros centros de investigación. De forma breve, se puede destacar la vacuna desarrollada por la farmacéutica Hipra situada en Girona y que comenzará sus ensayos clínicos en agosto junto al Hospital Clínic de Barcelona y en el Trueta de Girona.
Tres proyectos de vacunas españolas muy prometedoras
A continuación, se desgrana cada uno de los proyectos que tiene el CSIC en marcha, haciendo una pequeña aproximación de cómo funciona cada una de las vacunas.
Como veréis, ninguna de ellas emplea la tecnología de ARN mensajero, las cuales ya expliqué en el post «¿Qué son las vacunas de ARNm y cómo funcionan?«. No por esto son vacunas peores o mejores, simplemente se basan en otras técnicas que precisan de un mayor tiempo de desarrollo. Esto también elimina la idea de que están más investigadas que el resto y por tanto son más seguras. No es así. Además, en España, ha habido menos inversión, lo que ha supuesto un proceso de realización y desarrollo mucho más lento.
Proyecto de Vicente Larraga
El equipo de Vicente Larraga del Centro de Investigaciones Biológicas Margarita Salas (CIB-CSIC) está desarrollando una vacuna basada en ADN recombinante (sintetizado en el laboratorio). Esta tecnología permite obtener una vacuna más estable a temperatura ambiente en comparación a las que emplean ARN. Esta diferencia de estabilidad es una cuestión físico-química de las propiedades intrínsecas de las moléculas de ADN y ARN, muy diferentes entre sí. Que esta vacuna se base en ADN y sea más estable implica una gran ventaja en lo referente a aspectos logísticos, tanto de fabricación, como de distribución y administración.
Para hacer posible esta vacuna se ha utilizado un plásmido, una molécula circular de ADN que transporta el gen de interés (Figura 1). Este plásmido fue empleado por el mismo grupo de investigación que desarrolló una vacuna contra la leishmaniosis canina. Este hecho nos asegura que el plásmido está libre de secuencias que puedan resultar tóxicas, dado que ya se aprobó su uso en animales. Además, puesto que la base para la construcción del plásmido estaba ya hecha, el grupo de investigación se ha permitido una mayor rapidez en el desarrollo de la vacuna, ya que sólo han necesitado adaptarla a las secuencias de genes del nuevo coronavirus contra el que queremos inmunizarnos.
El uso de un plásmido sintético de ADN permite integrar el gen del antígeno escogido del organismo infeccioso, en este caso el que codifica para la proteína S (Spike o Espícula) y otras proteínas específicas del SARS-CoV-2. De esta forma, una vez se administre la vacuna, el plásmido entra en las células presentadoras de antígenos que serán capaces de producir la proteína S, siguiendo el dogma central de la biología molecular: el ADN se transcribe en ARN y éste se traduce a proteína (Figura 1B). Cuando la célula tenga sintetizada la proteína, la expondrá en su membrana para que células del sistema inmunitario (principalmente linfocitos T y linfocitos B) elaboren una respuesta adecuada frente a ella y se genere protección, en forma de memoria inmunológica (Figura 1C).
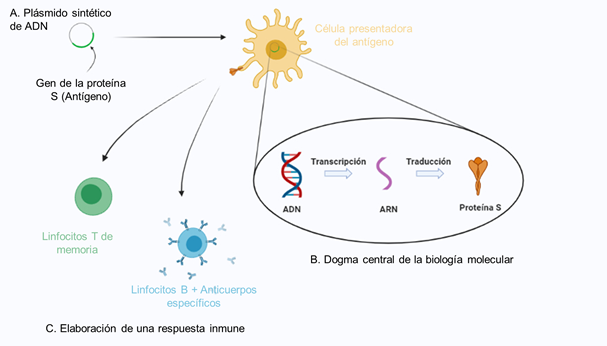
Por si surgen dudas, estas vacunas no pueden modificar nuestro material genético puesto que el funcionamiento del plásmido empleado es proporcionar las instrucciones para la proteína S encargada de generar inmunidad específica. Nunca se va a integrar, es decir, introducir en nuestro ADN dado que su acción es independiente y alejada del núcleo. Por último, cabe mencionar que, dado que la vacuna es de ADN, existe una gran facilidad para rediseñarla si no es efectiva ante una nueva variante.
Proyecto de Mariano Esteban
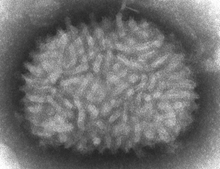
El equipo de Mariano Esteban pertenece al Centro Nacional de Biotecnología (CNB-CSIC). La vacuna que desarrollan consta del uso de un virus muy atenuado como vehículo de transporte (lo que en términos científicos se denomina vector vírico). Están empleando el virus Vaccinia (MVA, Figura 2) (García-Arriaza y Esteban, 2014), un poxvirus usado en su día para erradicar la viruela. Sí, las vacunas a largo plazo pueden conseguir esto, eliminar completamente de la faz de la Tierra la presencia de un patógeno.
El vector vírico transporta en su interior secuencias de ADN (Figura 3A) que producen, de nuevo mediante el dogma central de la biología molecular (Figura 3B), la proteína S del coronavirus, SARS-CoV-2. Estas proteínas se liberan al medio y son detectadas por las células presentadoras de antígenos que inducen al sistema inmunitario a elaborar una respuesta adecuada frente a ella, generando anticuerpos específicos (por parte de los linfocitos B) y linfocitos T de memoria (Figura 3C).
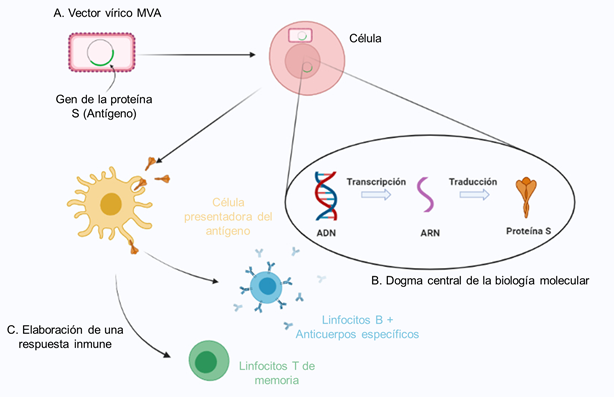
El hecho de emplear un vehículo basado en un virus atenuado (el virus MVA) resulta ventajoso puesto que la vacuna conseguirá acceder a muchos tipos celulares de forma muy fácil. Ocurre así dado que todos los virus poseen llaves específicas que facilitan la entrada en las células hospedadoras, puesto que sólo viven y se desarrollan dentro de estas. También hay que destacar que estas vacunas son bastante más estables que las basadas en ARNm.
Dentro de las vacunas desarrolladas por el CSIC, esta es la más avanzada y está demostrando tener un 100% de efectividad en animales de experimentación. Por ello, están preparando la producción a gran escala para comenzar los ensayos clínicos en humanos. Nos encontramos ante la candidata española más cercana a su comercialización masiva, una vez se haya avanzado los ensayos clínicos.
Esta vacuna MVA-COVID-19, debido a su alta atenuación y, dada la experiencia que el grupo de investigación tiene con la vacuna desarrollada contra la viruela, es probable que pueda administrarse a todo tipo de población incluyendo personas con inmunodeficiencias. Esto es importante, ya que las vacunas que emplean vectores víricos, pueden generar problemas graves en personas inmunodeprimidas, aquellas cuyo sistema inmune está debilitado. Además, la experiencia del grupo CNB-CSIC con vacunas previas similares a partir de MVA para Ébola, Chikungunya y Zika, sugieren que podría ser una vacuna con un alto grado de protección y muy extensa en el tiempo.
Proyecto de Luis Enjuanes e Isabel Sola
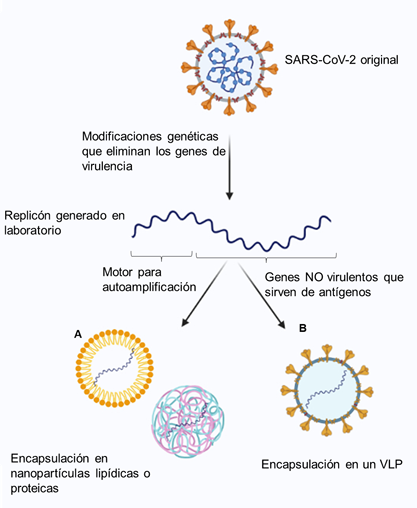
Quizá uno de los proyectos más novedosos a nivel mundial. El equipo de Luis Enjuanes e Isabel Sola, también del Centro Nacional de Biotecnología (CNB-CSIC), ha desarrollado lo que denominan virión sintético. Este surge a partir de muchas modificaciones del coronavirus original (SARS-CoV-2), causante de la COVID-19. Así pues, mediante ingeniería genética han eliminado los genes de virulencia del virus, de tal modo que lo han incapacitado suprimiéndole las armas que emplea para infectar nuestras células y dañarlas, así como las que permiten que se transmita con tanta facilidad. En resumen, han hecho una copia perfecta del virus, pero desarmado y se han mantenido aquellos genes que proporcionan inmunidad, es decir, los que generan antígenos como la proteína S (no siendo ésta la única que se incluyen).
El virión sintético ha derivado en una molécula de ARN con capacidad de autoamplificarse en la célula humana (huésped) hasta 5 mil veces más que las actuales vacunas, esto es un replicón de ARN. Esta capacidad se adquiere gracias a que contiene el motor que aumenta la producción de esos antígenos, los genes de la ARN polimerasa, enzima encargada de la función de transcripción de genes, es decir, de realizar parte del proceso de fabricación de todas las proteínas. Es justo la creación de esta molécula lo que hace que la candidata a vacuna sea una novedad, puesto que generar miles de copias permite elaborar una respuesta más amplia y potente.
En el siguiente esquema (Figura 4), se explica de forma muy resumida cuál es el fundamento de este proyecto. Asimismo, se expone las dos versiones en cuanto a la encapsulación del replicón generado, ya que tiene que envolverse en una capa protectora para poder entrar en la célula. La primera, e idea principal, es emplear nanopartículas bien de naturaleza lipídica (como las actualmente empleadas en las vacunas de ARNm) o bien con una tecnología basada en aminoácidos (Figura 4A). Como alternativa, cabe la posibilidad de usar un Virus Like Particles (VPL), que es una estructura similar al virus, con un combinado de proteínas sin capacidad de diseminarse una vez dentro del organismo (Figura 4B).
Los genes que conforman el replicón van a generar, de la misma forma que las vacunas basadas en ARNm o ADN (como la de Vicente Larraga), los antígenos de los que queremos protegernos. Además, como he dicho, el replicón permite que la dosis inyectada genere en nuestras células entre mil y 5 mil copias más del antígeno (o antígenos) del cual (o cuales) queremos protegernos. Esto generaría una mayor inmunidad que podría llegar a ser esterilizante, es decir, las personas vacunadas no enfermarían ni trasmitirían el virus. Ocurre así dado que las copias de antígenos generadas han permitido elaborar una memoria inmunológica más potente, generando más linfocitos B encargados de producir anticuerpos y más linfocitos T de memoria que coordinan la respuesta inmunitaria tras un segundo contacto con el virus.
Otro de los objetivos novedosos que persigue esta candidata es que la administración sea intranasal, lo que puede proporcionar una mayor protección en las vías respiratorias altas, la principal puerta de entrada del coronavirus a nuestro cuerpo. Así pues, se consigue una inmunidad local, que proporciona otro tipo de anticuerpos (IgA) que se secretan en las mucosas y protegen de la infección y diseminación del coronavirus en nuestro organismo.
Importancia de la proteína S
Si has estado atento, habrás comprobado que todas las vacunas trabajan con las secuencias de genes que sintetizan la proteína S. Y es que se sabe que esta proteína, presente en la superficie del SARS-CoV-2 (Figura 5A), es la encargada de permitir el acceso en nuestras células (células huésped) y por tanto una de las primeras en entrar en contacto con nuestro cuerpo (Figura 5B).

Por esto, resulta imprescindible hacer que nuestro cuerpo guarde una imagen de esta proteína para que cuando «se choque» en una posible infección con el virus original, elabore una respuesta inmunitaria a tiempo, antes de que éste haga de las suyas y desencadene graves problemas.
Conclusión
En España se está realizando muy buena ciencia y grandes avances en cuanto a la producción de vacunas para frenar esta pandemia. Algunas con unas ideas que pueden parecer simples y, otras que son una auténtica novedad y revolución. Estoy seguro de que tarde o temprano llegarán las tres a comercializarse y a estar a disposición de toda la población. Aunque, cada vez más personas están vacunadas a nivel mundial ni mucho menos estamos cerca de cubrir la totalidad. Por este mismo hecho es imprescindible que sigan apareciendo nuevas vacunas.
Para reflexionar…
Me gustaría acabar este artículo haciendo un poco de crítica ante la precaria situación de la ciencia en España. Las instituciones del CSIC son entidades públicas que se financian con recursos públicos. Sin embargo, nunca se ha invertido gran cantidad de dinero en estos centros. Esto siempre ha sido un problema para el desarrollo de muchas investigaciones en España, pero ha tenido un mayor impacto en estos dos últimos años, y España se ha quedado sin posibilidad de lanzar una vacuna a tiempo.
En una entrevista a Vicente Larraga, este afirmó que “sabemos que no podemos competir con las multinacionales, sería estúpido por nuestra parte”, confirmando lo que muchos sabíamos, que las grandes compañías que ahora tienen presencia en el mercado “han tenido 200 millones de ayuda de dinero público para hacer la vacuna y son 100, nosotros somos 13 o 15 y tenemos 700.000 euros. No es que no sepamos, es que, si tienes más dinero y medios, lo haces más rápido y compites mejor”.
Por fortuna, a la vista de las últimas noticias que publica el CSIC, una galerista, Helga de Alvear, ha hecho uno de los mayores aportes de dinero a uno de estos tres proyectos. Me resulta curioso que sea una persona la que, por cuenta propia y a nivel privado, haya hecho una de las aportaciones económicas más grandes para el desarrollo científico de una vacuna contra el coronavirus desarrollada en una entidad pública.
Todo este desarrollo científico hecho en España no vale para “llenarse la boca” de elogios. Si de verdad importa, no se debería hacer la vista gorda ante la grave situación en la que se encuentra la investigación española. Hay que hacer un pequeño gran esfuerzo por invertir mucho más en ciencia. Toda la comunidad científica advierte “sin ciencia no hay futuro” y esto es un hecho que ahora más que nunca se está viendo.
Artículo editado por Javier Sánchez y revisado por Carmen de Jesús Gil.
Artículos que pueden interesarte
- ¿Qué es la técnica PCR (Reacción en cadena de la polimerasa)?
- ¿Cómo afecta la pandemia a la propagación de la gripe?
- ¿Los virus están vivos o muertos? Los viriones
- ¿Quién es el causante de las pandemias? Enfermedades zoonóticas
Bibliografía
García-Arriaza J., and Esteban M. (2014). Enhancing poxvirus vectors vaccine immunogenicity. Human vaccines & immunotherapeutics, 10(8), 2235-2244.
Además, para la información sobre el desarrollo y funcionamiento de las vacunas se han revisado las siguientes páginas web oficiales:
Consejo Superior de Investigaciones Científicas (CSIC), (https://www.csic.es/en/palabras-clave/coronavirus)
Centro Nacional de Biotecnología (CNB-CSIC), (https://www.cnb.csic.es/index.php/es/investigacion/investigacion-sars-cov2)