Introducción
Imagínate una calurosa noche de verano, en la que no puedes dormir y dejas la ventana abierta para que haya corriente en la habitación. Pero, al abrigo de la noche, un visitante muy molesto hace acto de presencia. Zumban alrededor de tus orejas, producen picaduras y te despiertan. Por supuesto, hablo del mosquito. Aunque los mosquitos que te puedan picar durante la noche y no causen más problemas que los mencionados, existen otros mucho más peligrosos. Algunos trasmiten una peligrosa enfermedad llamada malaria o paludismo. Y no es para menos, ya que, actualmente, es una de las enfermedades más mortales que existen.
Pero, ¿qué es exactamente la malaria y qué mosquitos la transmiten? ¿Existe cura para tratar esta peligrosa enfermedad? Te invito a leer este artículo donde encontrarás las respuestas a estas preguntas y más. ¡Empecemos!
¿Qué es la malaria o el paludismo?
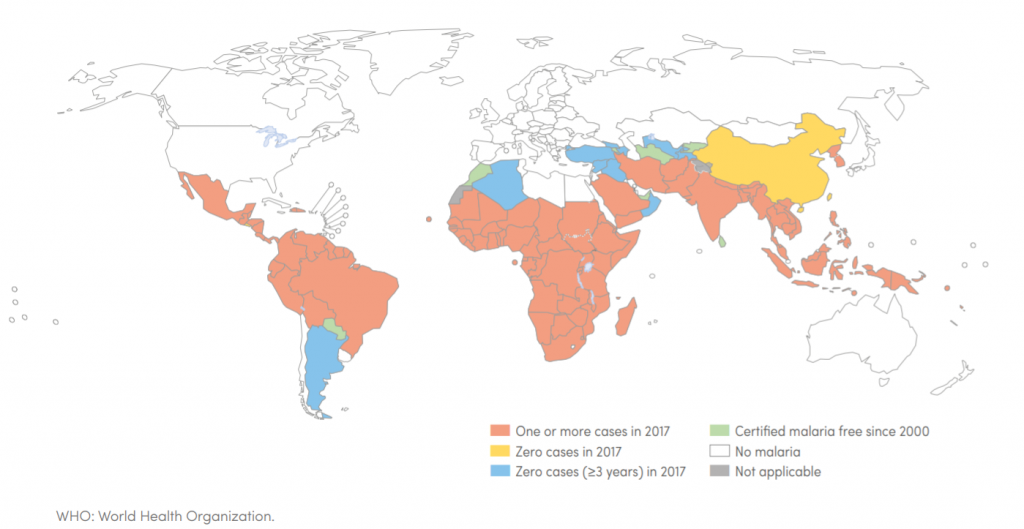
La malaria o paludismo es una enfermedad causada por protozoos parásitos, es decir, un organismo unicelular microscópico que vive a expensas de otro ser vivo. Concretamente los protozoos causantes de la malaria pertenecen al género Plasmodium, conocidos también como plasmodios. Estos plasmodios son sumamente peligrosos, ya que infectan a millones de personas al año, matando a cientos de miles de ellas. La Organización Mundial de la Salud (OMS) estimó que en el año 2017 hubo 219 millones de infectados, de los cuales alrededor de 435.000 murieron. Además, la mayoría de fallecimientos se registran en niños de entre 0 y 5 años. Espeluznante, ¿verdad?
La enfermedad está causada por la introducción de estos parásitos en el torrente sanguíneo, mediante un vector animal, en este caso el mosquito del género Anopheles. Allí encuentran los glóbulos rojos, los cuales utilizan para reproducirse y ocultarse del ataque del sistema inmune. Los glóbulos rojos o hematíes son las células de la sangre encargadas de transportar el oxígeno y el dióxido de carbono desde los alvéolos a las células, y viceversa. El plasmodio después de multiplicarse rompe el glóbulo rojo, causando una anemia grave. Además, la infección cursa con fiebre alta causada por diversos pirógenos endógenos, que son sustancias liberadas por la activación de células del sistema inmunitario (macrófagos y monocitos) a la circulación.
Tipos de plasmodios
Existen varias especies de plasmodios principales involucrados en la malaria. La inmensa mayoría se concentran en África, Centro y Sudamérica y el Sureste Asiático. El más conocido de ellos es Plasmodium falciparum, el agente causante de la malaria clásica (alrededor del 99 % de los casos registrados en todo el mundo). Otros parásitos son Plasmodium vivax y Plasmodium ovale, que producen una fiebre regular y periódica, clínicamente llamada terciana, con picos febriles cada 48 horas. Finalmente Plasmodium malariae produce fiebre cuartana, con picos cada 72 horas.
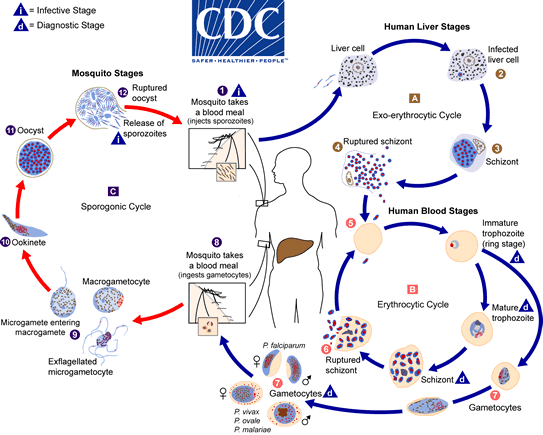
El ciclo de vida del parásito de la malaria
Los ciclos de vida de los protozoos parásitos, en su mayoría, implican el desarrollo de diferentes estadios o fases. Existen tres fases principales: una fase en el vector mosquito, una fase hepática inicial o fase pre-eritrocítica y una fase eritrocítica. Cabe destacar que este parásito necesita dos organismos anfitriones para completar su ciclo de vida: el mosquito, para las fases de reproducción sexual, y el ser humano u otro animal, para la reproducción asexual.
Fases hepática y eritrocítica
Todo comienza cuando un mosquito hembra del género Anopheles previamente infectado por el P. falciparum se alimenta de la sangre de una persona sana e inyecta en ella los esporozoitos. Y sí, digo hembra, ya que son las únicas que se alimentan de sangre para poder criar su progenie. La forma del parásito llamada esporozoito es la que se desarrolla en el interior del vector y, a su vez, es la que inicia nuevamente el ciclo.
Una vez en la sangre, los esporozoitos se dirigirán al hígado, donde infectarán las células hepáticas (hepatocitos). Así dará comienzo a la fase hepática o fase pre-eritrocítica. Los esporozoitos se multiplicarán mediante división asexual dentro de los hepatocitos, dando lugar a miles de formas del parásito llamados merozoitos.
Tras un tiempo, los merozoitos abandonarán el hígado para dirigirse a la sangre de nuevo, comenzando la fase eritrocítica. Allí atacarán y destruirán los glóbulos rojos mientras se multiplican, dando lugar a su vez a la forma de trofozoito. El trofozoito es la forma vegetativa del parásito, que se reproduce y se alimenta dentro de los glóbulos rojos. Parte de los merozoitos no se reproducirán sino que se transformaran en las células sexuales del parásito, llamados gametocitos.
Existe una excepción en este proceso con las especies P. vivax y P. ovale. Ambas son capaces de crear una forma enquistada de esporozoitos dentro de los hepatocitos, conocidas como hipnozoitos. Éstos permanecen latentes durante un tiempo determinado en los hepatocitos y son las responsables de causar síntomas varios meses después de la infección, conocidas como recidivas.
Fase en el vector mosquito
Cuando otro mosquito hembra pique y succione la sangre infectada que contiene los gametocitos, comenzará la fase de reproducción en el mosquito. Estos gametocitos o formas sexuales del parásito se someten a una unión sexual en el intestino medio del mosquito hembra. Es decir, se forma un ovoquiste o “huevo gigante” donde se producen de nuevo los esporozoitos. Esta forma del parásito es infectiva y alcanzan las glándulas salivares del mosquito. Una vez allí estarán preparados para infectar a otro ser humano y comenzar el ciclo de nuevo.
¿Cómo combatimos la malaria?
Existen diferentes métodos que intentan combatir al parásito causante de la malaria. Algunos métodos se centran en atacar directamente al vector de transmisión, es decir, al propio mosquito. Una de las técnicas más novedosas es el denominado gen-drive. Otros métodos incluyen el uso de drogas antimaláricas como la famosa quinina y sus derivados. Esta droga es el compuesto más antiguo utilizado para tratar las fiebres de la malaria. Otra droga famosa utilizada durante la Segunda Guerra Mundial fue, por ejemplo, la mepacrina (comercializada como Atabrine).

Tipos de fármacos contra la malaria
Los fármacos antimaláricos se clasifican en tres grandes grupos: los compuestos de arilaminas, (donde se incluyen drogas como la quinina, cloroquina y mefloquina), los compuestos de antifolatos y los compuestos de artemisinas.
La mayoría de los fármacos atacan al parásito en su forma eritrocítica asexual o merozoito, aunque existen drogas más específicas. Algunos fármacos denominados esquizonticidas atacan las formas de hipnozoitos hepáticos, evitando así recidivas en el paciente enfermo. Otros fármacos son gametocidas, es decir, destruyen las formas sexuales del parásito o gametocitos, evitando así que el parásito llegue al mosquito vector. Finalmente los fármacos esporontozidos bloquean la formación de los esporozoitos dentro del mosquito, evitando así que infecten a individuos sanos.
Pero, al igual que los virus y las bacterias, tanto los plasmodios como el mosquito Anopheles pueden desarrollar resistencia contra los medicamentos antimaláricos. La cloroquina ha sido el fármaco más utilizado para tratar la malaria, pero su uso descontrolado ha provocado la aparición de resistencias desde los años 50. Otras mutaciones en genes claves del parásito han producido la aparición de resistencias frente a la quinina y la mefloquina también.
En resumen, la elevada capacidad de mutación del parásito, una gran carga parasitaria, la potencia del fármaco seleccionado, la mala adherencia al tratamiento, el uso masivo de fármacos, una inadecuada dosificación de las medicinas y el uso de fármacos con propiedades inadecuadas son las principales razones por las que han aparecido resistencias a lo largo de las últimas décadas.
¿Y las vacunas contra la malaria?
La existencia de diferentes fases de desarrollo del parásito nos puede brindar cierta ventaja, ya que se puede bloquear ese desarrollo en diferentes puntos de la cadena. Es por eso que los investigadores han desarrollado vacunas contra la fase pre-eritrocítica o hepática, contra la fase eritrocítica y otras que bloquean la transmisión. También se pretenden crear vacunas contra múltiples fases de la malaria. Pero, ¿en qué se diferencian exactamente estas vacunas? Veámoslo.
Vacunas contra la fase pre-eritrocítica o hepática
Tal y como su nombre lo sugiere, estas vacunas tienen como objetivo atacar las células del plasmodio que se encuentran en el hígado. Concretamente están dirigidas a atacar los merozoitos, es decir, las células que posteriormente infectarán los glóbulos rojos de la sangre.
Vacunas contra la fase eritrocítica
Estas vacunas están dirigidas a combatir las células denominadas merozoitos. Estas células son las que infectan y destruyen los glóbulos rojos de la sangre. Las vacunas de este tipo también están diseñadas para destruir o marcar los glóbulos rojos infectados, para así detener el ciclo del parásito.
Vacunas que bloquean la transmisión
Mediante el uso de estas vacunas se pretende destruir las formas sexuales o gametocitos del parásito, y así evitar que éstos sean ingeridos por los mosquitos. Al destruirse estas células se evita que los mosquitos se infecten y expandan la enfermedad.
Vacunas contra multiples fases de la malaria
Estas vacunas pretenden atacar al parásito en sus diferentes formas. Están pensadas principalmente para atacar a las formas eritrocitarias y hepáticas. La vacuna AMA1 es uno de los pocos ejemplos disponibles que existen. Pero existe un importante problema que los científicos tienen que abordar, y es la selección del antígeno adecuado, esto es la molécula contra la que dirigir las vacunas para activar al sistema inmunitario. No hay muchos antígenos que se presenten en las diferentes fases de desarrollo del parásito.
La solución puede consistir en combinar diferentes vacunas o subunidades de las vacunas, para así poder formar una respuesta inmunitaria conjunta. Aunque la idea parezca evidente, en la practica es difícil de aplicar. Este tipo de vacunas suponen el uso de diferentes adyuvantes (sustancias que ayudan a activar el sistema inmunitario), además de incrementar mucho el tiempo y coste de la producción de los diferentes componentes. De momento las investigaciones se centran en bloquear al parásito en una de sus diferentes fases de desarrollo.
Estado actual de las vacunas contra la malaria
A pesar de que se hayan desarrollado un gran número de vacunas diferentes, solo una demuestra resultados medianamente aceptables. Se trata de la vacuna RTS,S/AS01, comercializado como Mosquirix. Es una vacuna desarrollada en contra de la fase pre-eritrocítica del parásito. Los resultados del ensayo de la fase III fueron publicados en First results of phase 3 trial of RTS, S/AS01 malaria vaccine in African children. En los ensayos de fase III se busca verificar la eficacia del fármaco y la seguridad, y los ensayos suelen incluir a un mayor número de participantes (entre 300 y 3000).

La vacuna RTS,S/ AS01 es una proteína recombinante, formada por la proteína CSP que se expresa en los esporozoitos de la fase hepática, el antígeno superficial del virus de la hepatitis B y el adyuvante AS01. El adyuvante tiene como función la de potenciar aún más la respuesta del sistema inmunológico. Esta vacuna está diseñada para atacar a la especie Plasmodium falciparum, la más peligrosa de todas.
Específicamente, la vacuna hace que el sistema inmune detecte la proteína CSP, que es la proteína más importante que cubre el esporozoito. Como resultado, se producen anticuerpos específicos son capaces de neutralizar al parásito antes de que infecte los hepatocitos, uniéndose y bloqueando dicha proteína. También es importante señalar que, además de anticuerpos, la vacuna induce una respuesta de linfocitos T CD4+. Este tipo de linfocitos se denominan colaboradores, y su función es coordinar las diferentes respuestas del sistema inmunológico, entre otras.
El ensayo se realizó desde Marzo del año 2009 hasta Enero del año 2011 y participaron un total de 15.460 niños de entre 6 semanas y 17 meses de edad. Los infantes recibieron hasta tres dosis de la vacuna y un refuerzo a los 18 meses del estudio. El primer análisis se realizó a los 14 meses en 6000 niños y se comprobó que la eficacia de la vacuna fue de un 55,8 %. En cambio, la eficacia contra la malaria severa fue de un 47,3 %. No obstante, teniendo en cuenta todos los grupos de edad, se estimó que la eficacia de la vacuna fue de un 34,8 %.
Actualmente, tras haber vacuna a más de 800.000 niños en Ghana, Kenya y Malawi desde 2019, la OMS ha recomendado la administración generalizada de la vacuna vacuna RTS,S a la población infantil del África Subsahariana y de otras regiones donde la transmisión de Plasmodium falciparum sea moderada o alta.
La vacuna RTS, S es la única vacuna autorizada hasta la fecha y ha demostrado una moderada eficacia. La recomendación de su uso en niños es un momento histórico en la lucha contra la enfermedad e infunde nuevas esperanzas en las miles de personas que la sufren cada año.
Su uso, junto con otros métodos de control y prevención de la malaria, es bastante eficaz para controlar, particularmente, la malaria severa y la malaria endémica. Afortunadamente, las nuevas tecnologías van a permitir descubrir y testar nuevos antígenos contra la malaria. Además, se están investigando nuevos tipos de adyuvantes, capaces de potenciar aún más la respuesta inmune.

¿Qué has aprendido?
Tal y como habrás podido ver, la enfermedad de la malaria es más complicada de lo que parece. Esto es debido a la extensa presencia de su vector en las zonas tropicales, el mosquito Anopheles hembra y a su difícil erradicación. Además existen diferentes especies de plasmodios, de los cuales el más peligroso es P. falciparum, y que presenta diferentes estados de desarrollo.
Lo peor de todo es que a pesar de los años de investigación aún no se ha desarrollado una vacuna realmente efectiva. Esperemos que dentro de unos años la ciencia descubra una cura para reducir los efectos de esta enfermedad tan mortal que afecta especialmente a los niños.
Si te ha gustado el articulo ¡No dudes en compartirlo! Desde aquí también te invito a leer los demás excelentes artículos que encontrarás en el blog, donde aprenderás un montón sobre las ciencias biológicas.
Artículo editado por Javier Sánchez.
Artículos que pueden interesarte
- Los postulados de Koch. En busca del causante de la enfermedad.
- La levadura como organismo modelo en investigación.
- Basquilla y la bacteria Clostridium perfringens
- Magnetosomas: brújulas microbiológicas
Bibliografía
RTS, S Clinical Trials Partnership. (2011). First results of phase 3 trial of RTS, S/AS01 malaria vaccine in African children. New England Journal of Medicine, 365(20), 1863-1875.
RTS,S Clinical Trials Partnership. Efficacy and safety of RTS,S/AS01 malaria vaccine with or without a booster dose in infants and children in Africa: final results of a phase 3, individually randomised, controlled trial [published correction appears in Lancet. 2015 Jul 4;386(9988):30]. Lancet. 2015;386(9988):31-45. doi:10.1016/S0140-6736(15)60721-8
WHO. Q&A on the malaria vaccine implementation programme (MVIP).
Meibalan, E., & Marti, M. Biology of malaria transmission. Cold Spring Harbor perspectives in medicine. 2017; 7(3).
Wilson, K. L., Flanagan, K. L., Prakash, M. D., & Plebanski, M. (2019). Malaria vaccines in the eradication era: current status and future perspectives. Expert review of vaccines, 18(2), 133-151.
World Malaria Report 2018. Geneva: World Health Organization; 2018. Licence:
CC BY-NC-SA 3.0 IGO.
Shibeshi MA, Kifle ZD, Atnafie SA. Antimalarial Drug Resistance and Novel Targets for Antimalarial Drug Discovery. Infect Drug Resist. 2020;13:4047-4060. Published 2020 Nov 10. doi:10.2147/IDR.S279433
https://www.who.int/es/news/item/06-10-2021-who-recommends-groundbreaking-malaria-vaccine-for-children-at-risk (última vez consultado 04/11/2021)