¿Ciencia-ficción o realidad? ¿Milagro o genética? La investigación biomédica puede ser muy dura, pero por el simple hecho de intentar proporcionar una vida mejor, ya merece la pena. Hace tres años presencié una charla científica de aquellas que emocionan y que me recordó cuánto amo la ciencia. Hoy quiero darte a conocer esta historia; te contaré el caso de Hassan, el niño mariposa que se curó gracias a la terapia génica.
Índice de contenido:
La piel de mariposa
Los “niños mariposa” padecen una afección genética rara conocida como enfermedad de la piel de mariposa, o Epidermólisis Bullosa. Esta patología se manifiesta durante la infancia y consiste en una malformación de las células de los tejidos superficiales como la piel, las cuales pierden su capacidad de mantenerse unidas. Esto hace que su piel sea tan frágil como las alas de una mariposa: cualquier roce, por mínimo que sea, crea ampollas y heridas relativamente profundas. En algunos casos esta enfermedad puede ser leve, pero 4 de cada 10 niños no llegan a la adolescencia.
Según datos de la ONG DEBRA, la Epidermólisis Bullosa tiene una prevalencia de 10 personas por cada millón de habitantes. En España existen aproximadamente 500 casos de piel de mariposa. La calidad de vida de los pacientes con esta enfermedad es muy baja: viven en constante dolor, y pequeñas acciones como caminar pueden ser extremadamente duras, por lo que deben aplicarse curas y vendajes constantemente. Incluso cuando comen, los trozos de comida pueden dañar la boca o el esófago del paciente con piel de mariposa. A día de hoy, no existe un tratamiento eficaz para las personas con piel de mariposa.
El caso de piel de mariposa de Hassan
Desde que nació en Siria, Hassan empezó a manifestar heridas en su piel causadas con mucha facilidad. Aunque se diagnosticó correctamente como piel de mariposa, los médicos no pudieron proporcionarle ninguna cura. Tras mudarse con su familia a Alemania, los médicos del país tampoco pudieron hacer nada por él. Sus padres estaban desesperados. En 2015, Hassan ingresó en el hospital pediátrico de la Universidad de Ruhr a cargo del doctor Tobias Hirsch, quien nunca había visto nada parecido: Hassan, con 7 años de edad, había perdido el 80% de su piel, y no le quedaba mucho por vivir.
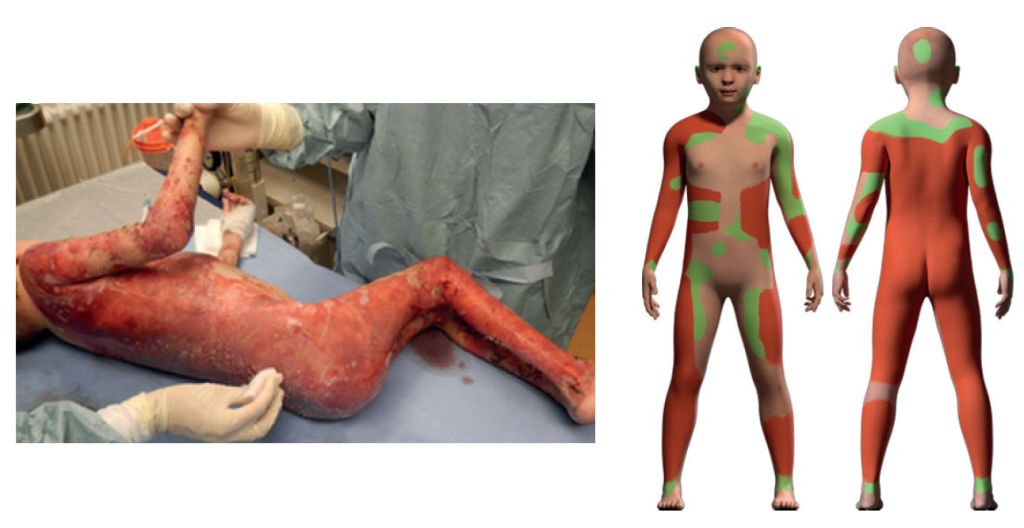
Epidermólisis Bullosa Juntural
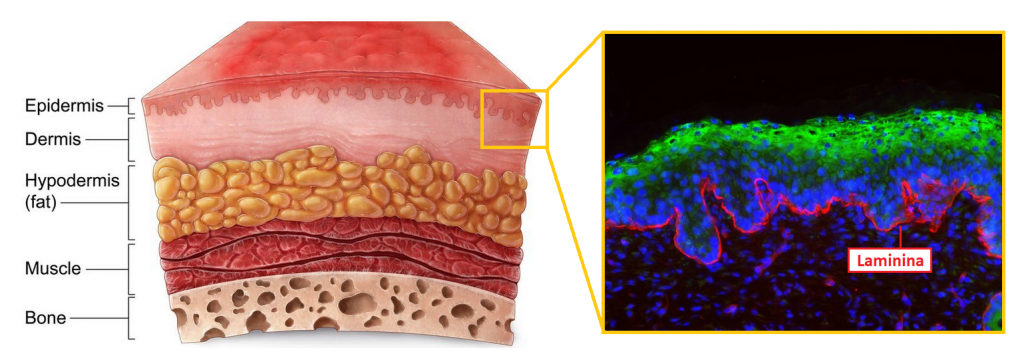
La piel humana se divide en tres capas principales: la epidermis (la capa más externa), la dermis y la hipodermis. Tras la hipodermis se encuentra el músculo y, finalmente, el hueso. La enfermedad de piel de mariposa de Hassan pertenece a la categoría de Epidermólisis Bullosa Juntural, una patología genética que afecta las dos primeras capas de la piel: la epidermis y la dermis.
En particular, las células de Hassan tenían una mutación en el gen LAMB3, el cual es importante para la síntesis de una proteína llamada laminina. La laminina es relevante para la correcta formación de la membrana basal que une las células de la epidermis con las de la dermis. Esta unión es la que permite que dispongamos de una piel resistente contra las agresiones y los esfuerzos a los que se somete día a día. La mutación de la piel de mariposa de Hassan impedía la correcta formación de esta membrana basal, lo que hacía su piel extremadamente frágil.
Las mentes detrás de la operación
La única esperanza del doctor Hirsch fue contactar con el equipo del Profesor Michele de Luca. De Luca es investigador en la Universidad de Módena y Reggio Emilia, en Italia, y posee una larga experiencia en terapia génica. Por aquel entonces, de Luca había iniciado un ensayo clínico usando terapia génica en pacientes con piel de mariposa, por lo que aceptó el reto de curar a Hassan. Así pues, con el consentimiento de los padres del niño, el equipo italo-alemán se puso manos a la obra.

La terapia génica
La estrategia de Michele de Luca fue restablecer la funcionalidad del gen LAMB3 mediante terapia génica. La terapia génica consiste en la introducción de material genético en células humanas con intención curativa. En este caso, el plan fue introducir una copia sana del gen LAMB3, a fin de eliminar los efectos de la mutación de piel de mariposa de Hassan. Para ello, los investigadores tomaron células a partir de una muestra de la poca piel sana que le quedaba, y las pusieron en cultivo. Mediante el uso de virus, introdujeron el gen sano a las células, por lo que se pudo restablecer la correcta síntesis de laminina.
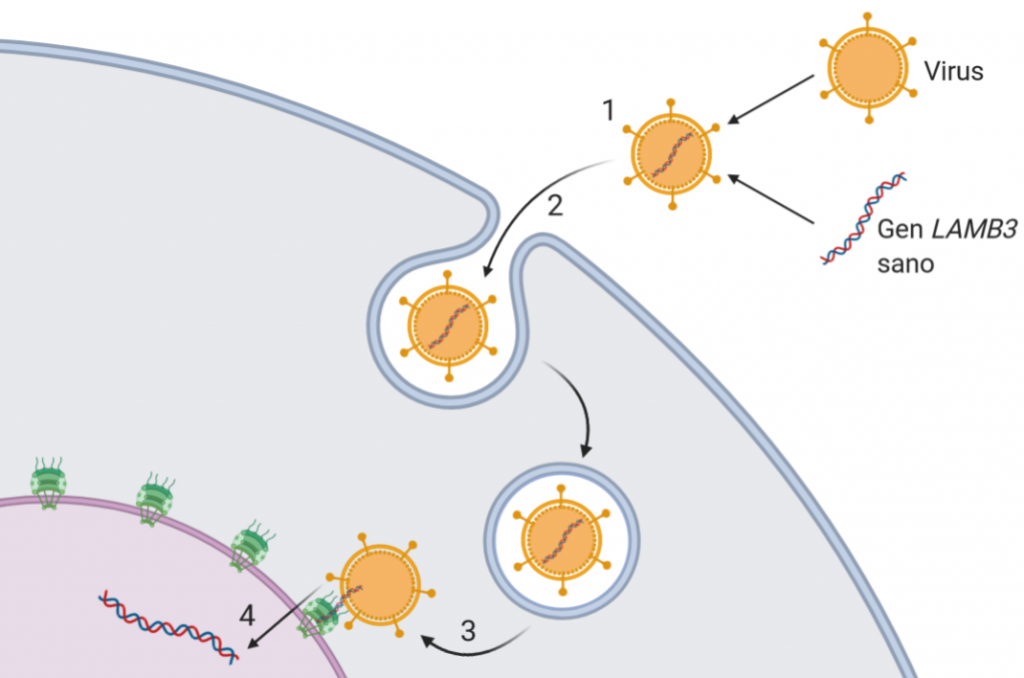
Al incorporar el gen sano en el ADN, un potencial problema podría haber sido el desencadenamiento de nuevas mutaciones. Además de usar un tipo de virus ya aprobado para su uso en el ensayo clínico liderado por de Luca, los investigadores analizaron las células resultantes y vieron que no solo la integración del LAMB3 sano había sido exitosa, sino que no presentaban ninguna alteración que hiciera peligrar la vida del niño.
Fábricas de piel «a la carta»
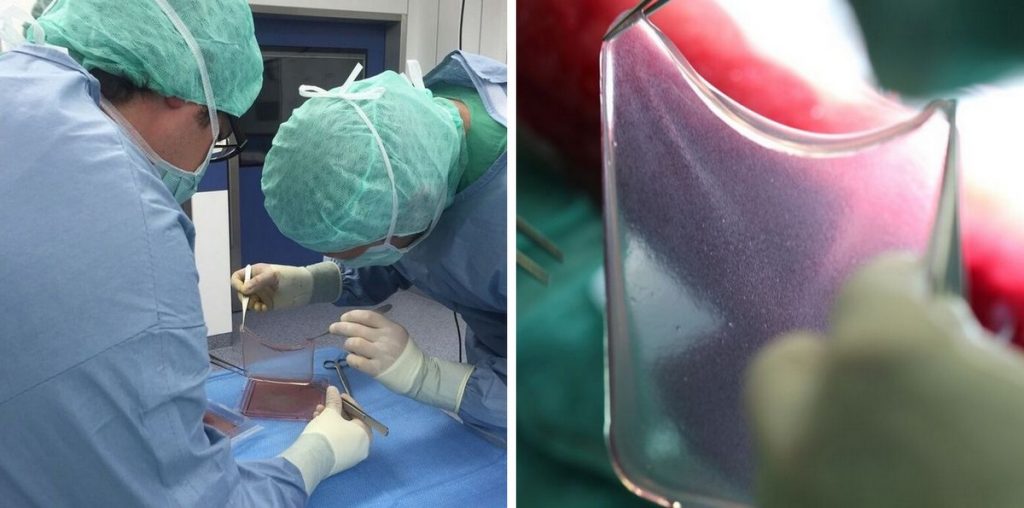
Usando estas nuevas células, los investigadores pasaron a fabricar la nueva piel de Hassan. En unas condiciones específicas, las células en cultivo pudieron proliferar y generar capas firmes de piel. ¡Se llegó a generar casi un metro cuadrado de piel sana! Una vez sintetizada, la aplicaron sobre la piel dañada de Hassan como si se tratara de parches. Cuando se analizó la nueva piel por microscopía, los investigadores vieron que las células modificadas eran capaces de sintetizar correctamente laminina, de modo que se pudo reconstruir la membrana basal que separa la epidermis de la dermis.
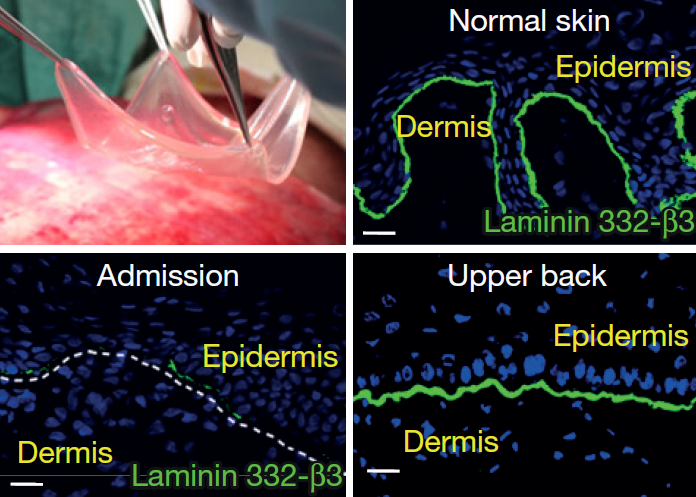
La cura de la piel de mariposa, una nueva piel para lucir
La mejoría fue asombrosa: al cabo de 4 meses, la piel sintética se expandió y regeneró por completo todas las áreas dañadas por la piel de mariposa. Cuando el equipo probó a rasgar y pellizcar a Hassan, la piel ya no se dañaba como sucedería normalmente en un paciente con piel de mariposa. Los meses pasaban y las nuevas células seguían sintetizando laminina sin problemas. Al cabo de dos años, Hassan logró tener la vida que nunca tuvo de pequeño e hizo realidad su gran sueño: jugar al fútbol. Así pues, el equipo logró una hazaña histórica en la biomedicina curando la piel de mariposa. Gracias a la terapia génica, no sólo salvaron la vida de un niño, sino que le regalaron la infancia que no pudo tener por culpa de su enfermedad.
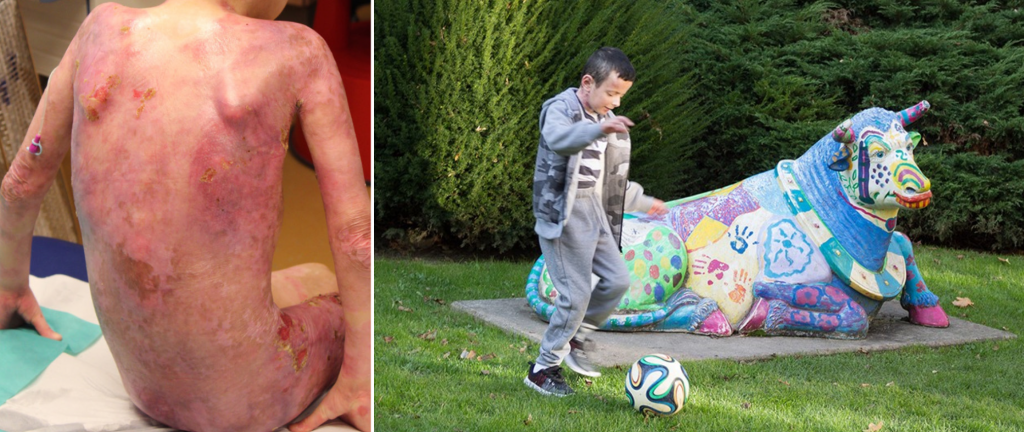
Reflexión final
La investigación biomédica intenta dar solución a enfermedades complejas como la piel de mariposa que no se pueden tratar con los medicamentos de que disponemos hoy en día. Cada vez más, aparecen nuevos tratamientos en fase de investigación muy prometedores. Aunque estos todavía no estén en el mercado, se pueden usar en casos extremos.
Del mismo modo que ya argumenté en mi anterior artículo, la prioridad de los científicos en biomedicina es curar a los enfermos. El caso de Hassan es un buen ejemplo: por su tipo de mutación, en principio quedaba excluido del ensayo clínico del Profesor de Luca. Sin embargo, debido a que no existe otra cura y al tratarse de un caso de vida o muerte, se le permitió beneficiarse de la terapia génica experimental. Esto es lo que se conoce como un “uso compasivo” de las terapias en investigación, y se da en una gran variedad de ensayos clínicos en situaciones de extrema necesidad.
Por otro lado, en la última década se ha producido un salto enorme en el terreno de la ingeniería genética. En concreto, el auge de la tecnología CRISPR promete generar modificaciones genéticas más precisas que las que se logran usando virus. ¿Os imagináis poder curar enfermedades raras con tan solo una modificación sencilla, precisa y segura? Tal vez aún quede mucho trabajo por delante, pero no sería una sorpresa llegar muy pronto a alcanzar este hito.
Espero que hayáis disfrutado de este artículo. Para cualquier duda, escribid en los comentarios y os responderé encantado.
Artículos que pueden interesarte
- Páncreas a la carta: el futuro de la medicina regenerativa en el tratamiento de la diabetes
- La enfermedad de Parkinson. Hipocinesia, síntomas y tratamiento.ç
- ¿Cómo se descubre la causa genética de una patología?
- Insomnio familiar fatal: la enfermedad que no te deja dormir
Referencias
- Hirsch et al., «Regeneration of the entire human epidermis using transgenic stem cells». Nature, 2017.
- Mavilio et al., «Correction of junctional epidermolysis bullosa by transplantation of genetically modified epidermal stem cells». Nature Medicine, 2006.
- Clinicaltrials.gov, ensayo HOLOGENE7 (NCT02984085): «Clinical Trial to Assess Safety and Efficacy of Autologous Cultured Epidermal Grafts Containing Epidermal Stem Cells Genetically Modified in Patients With RDEB».
- Kat Arney: «Change the genes to fix the skin, the largest organ in the body is a prime target for gene therapy«. Nature Outlook, 2018.
- James Gallagher: «Butterfly child given life-saving skin». BBC News, 2017.
- Gary Finnegan: «The story of a new skin». Horizon Magazine, 2017.







