El páncreas es un órgano digestivo que secreta una amplia diversidad de sustancias que participan tanto en la digestión de los alimentos como en el metabolismo. El pancreas presenta una estructura aplanada de unos 12.5-15 centímetros de longitud y se ubica en la curvatura que se origina en el primer tramo del intestino delgado, conocido como duodeno. El 99% del pancreas está constituido por las células que participan en la digestión de los alimentos, mientras que el 1-2% restante de las células pancreáticas se organizan en lo que se conoce como islotes pancreáticos o islotes de Langerhans y que incluyen a los tipos celulares que participan en el metabolismo.
Se han identificado múltiples patologías que pueden afectar al pancreas, entre ellas, la pancreatitis o el cáncer pancreático. Sin embargo, la enfermedad mas extendida en la población y asociada al pancreas es la diabetes. Por ello, este artículo se centra en los tratamientos usados y el enfoque de las diferentes investigaciones que se están llevando cabo actualmente para conseguir curar esta patología.
Índice de contenido:
¿Qué es la diabetes?
La diabetes es un trastorno que afecta al metabolismo de la glucosa, que es la fuente principal de obtención de energía de nuestras células.
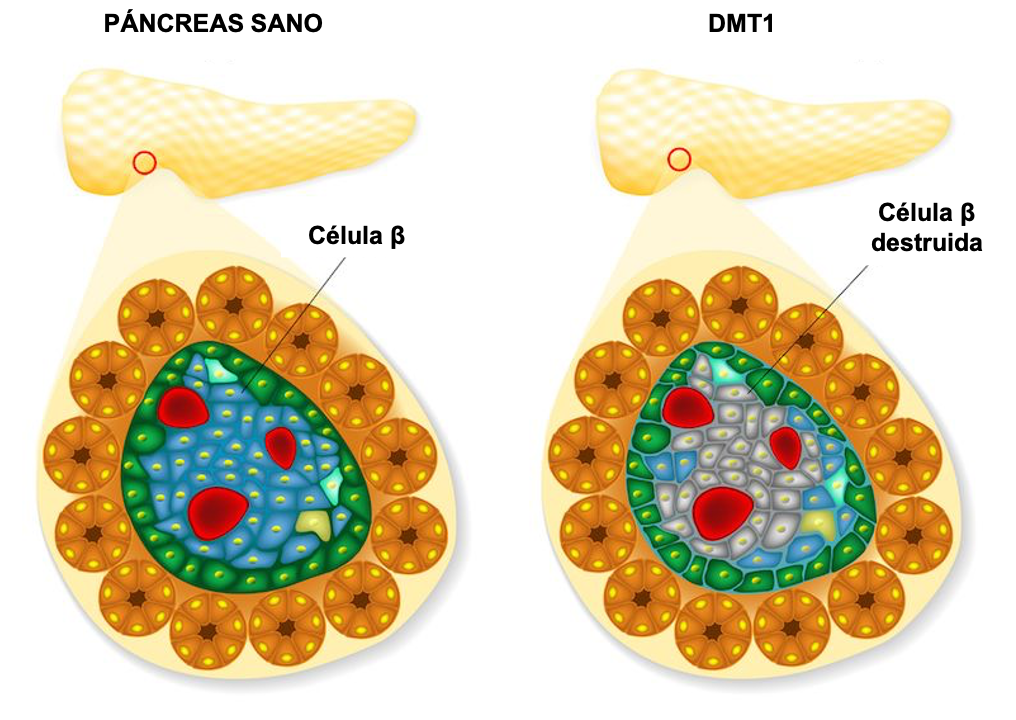
Los subtipos de diabetes que presentan mayor incidencia en la población son la diabetes mellitus tipo 1 (DMT1) y la diabetes mellitus tipo 2 (DMT2). La DMT1 es una de las variantes de esta enfermedad y puede presentarse en personas de cualquier rango de edad, pero se desarrolla por lo general en niños y adolescentes. Esta patología constituye un 10% de los casos totales de diabetes y se caracteriza porque el sistema inmune del paciente ataca y destruye las células que se encargan de la producción de la hormona insulina. Estas células productoras de insulina se ubican en los islotes pancreáticos y se les conoce como células beta. La DMT2 constituye el 90-95% de los pacientes diabéticos y las alteraciones metabólicas que desarrollan son diferentes a las de los pacientes de DMT1, ya que inicialmente no hay una destrucción de células pancreáticas.
Insulinoterapia en diabetes
La insulina es una hormona que se une a la membrana de la células de tejidos efectores, como el tejido hepático o el músculo esquelético entre otros. Esta unión permite la entrada de la glucosa desde la sangre al interior de las células de estos tejidos, pudiendo entonces usarla a modo de combustible energético.
Los pacientes de DMT1 carecen de células beta pancreáticas y, por tanto, no producen insulina. Por ello requieren un tratamiento de insulina o insulinoterapia para mantener a raya los niveles de glucosa en sangre o glucemia. Por esa razón, cuando en 1921 Frederick G. Banting, Charles Best, James Collip y el británico John J.R. Macleod consiguieron aislar por primera vez insulina canina, fue todo un hito en la historia de la medicina. Este hecho pasó a convertir a la DMT1, que hasta entonces había sido una enfermedad terminal, en una enfermedad tratable y crónica.
A pesar de todo, la insulinoterapia se considera un parche, ya que los pacientes de DMT1 presentan una esperanza de vida de hasta 12 años menos que el resto de las personas que no desarrollan la enfermedad. Esta menor esperanza de vida se debe a las complicaciones secundarias que se originan a largo plazo a causa de los niveles elevados de glucosa en sangre, como son daños en órganos relacionados con el sistema renal o el cardiovascular.
Es por esto que los científicos de todo el mundo siguen esforzándose en encontrar una cura para esta patología. Y las investigaciones se centran no en la búsqueda de mejorar las formas de aporte de insulina al cuerpo, si no en la forma de reemplazar las células beta pancreáticas destruidas por el sistema inmune.
Técnicas alternativas a la insulinoterapia
Algunos de los tratamientos o terapias que se están estudiando desde hace unos años y que son alternativos a la insulinoterapia son la terapia génica y la medicina regenerativa.
La terapia génica investiga la reprogramación de las células beta para evitar ser destruidas por el sistema inmune del paciente, mientras que la medicina regenerativa se basa en el reemplazo de células o tejidos con la finalidad de restaurar el funcionamiento normal del organismo.
Dentro de la medicina regenerativa se trabaja en dos vías: reemplazar las células beta pancreáticas con células de donante o bien obtener células beta a partir de células madre para transplantarlas en el paciente.
1. Trasplantes de células beta de donantes
Una de las técnicas que se lleva estudiando desde los años 80, consiste en el trasplante de células beta en pacientes con DMT1 procedentes de donantes con muerte cerebral. El cirujano James Shapiro pudo realizar esta técnica con éxito en siete pacientes en el año 1993, de los cuales uno no necesitó seguir con la terapia con insulina durante más 20 años.
En esta técnica los páncreas extraídos de los donantes se someten a un proceso de disociación mecánica y de purificación de los islotes pancreáticos, siendo incubados durante 24h antes de ser trasplantados. Los pacientes son sedados y los islotes se infunden mediante un abordaje transhepático percutáneo que permite crear un túnel a través del hígado y alcanzar así la vena porta, en donde se coloca un catéter para facilitar la introducción de los islotes de los donantes.
El problema de esta técnica, conocida como protocolo Edmonton, es que para evitar que el propio sistema inmune del paciente ataque nuevamente a las células “recién instaladas” deben someterse a una terapia inmunosupresora muy potente, lo cual genera un mayor riesgo de infecciones o complicaciones. Además, aunque miles de enfermos de DMT1 están deseando poder someterse a este tratamiento, actualmente el número de posibles donantes no cubre las necesidades, ya que se necesitan hasta cuatro donantes para obtener células beta suficientes para un solo paciente.
2. Obtención de células beta a partir de células madre
La otra técnica con la que se trabaja hoy en día es el uso de células madre para crear células “dispensadoras de insulina” en el laboratorio. Esto es posible porque las células madre tienen el potencial o capacidad de convertirse en cualquiera de los tipos celulares del cuerpo. Si se las estimula adecuadamente pueden convertirse en una célula de la piel, una célula muscular o una célula beta pancreática.
Estas células madre pluripotentes se obtienen de embriones de embarazos interrumpidos y tienen la peculiaridad de que a partir del cultivo de una sola célula se pueden obtener cientos y miles de células hijas gracias a la división celular.
Una de las técnicas empleadas en ViaCyte (compañía de medicina regenerativa centrada en el desarrollo y comercialización de terapias génicas) consistió en obtener células pancreáticas progenitoras e introducirlas directamente en ratones diabéticos. Tras 2-3 meses los ratones, con tratamiento de inmunosupresión incluido, empezaron a controlar sus niveles de glucosa en sangre. Esta técnica está siendo probada actualmente en ensayos clínicos con pacientes.
Entonces ¿dónde está el problema entonces?
El problema de introducir estas células progenitoras pancreáticas en un nuevo organismo sigue siendo el mismo. No sólo son células extrañas que el sistema inmune va a vigilar muy de cerca, si no que, además, el sistema inmune del paciente de DMT1 se caracteriza por rastrear y destruir especialmente cualquier tipo de célula beta pancreática.
Una de las soluciones, que plantearon las empresas biotecnológicas que lideran esta carrera por conseguir un tratamiento efectivo para la DMT1, es ocultar a las células introducidas en el organismo. Por ejemplo, encapsulándolas mediante un recipiente polimérico que actuara como barrera física. El problema de esto es que todas nuestras células necesitan acceso a oxígeno y nutrientes y, si se aíslan, éstos no llegan lo suficientemente bien a través de la sangre.
Otra de las soluciones con las que se trabaja es usar la ingeniería genética para crear unas «super-células» que eviten la detección por las células del sistema inmune, al igual que hacen las células del cáncer o las células fetales que evitan ser destruidas por el sistema inmunológico de la madre. Por el momento, las investigaciones al respecto se desarrollan sin mucha información por parte de los laboratorios que las llevan a cabo.
Conclusiones
En resumen, sea cual sea la solución, la carrera por ser el primero en encontrar la cura para la diabetes sigue en marcha. A día de hoy los pacientes de DMT1 requieren de tratamiento diario con insulina de por vida para controlar los niveles de glucosa, y cuentan con una menor esperanza de vida. Por lo que tanto la terapia génica como el trasplante de donantes supone un rayo de luz para estos pacientes.
Lo que está claro es que el equipo que alcance antes la meta no sólo obtendrá el reconocimiento en el mundo científico, si no que habrá hecho posible una mejora en la calidad de vida de más de 40 millones de personas que pelean día a día contra su propio metabolismo. Lo importante, en mi opinión, es que estos equipos de investigación no desvíen su objetivo y acaben vendiendo sus descubrimientos al mejor postor, ya que la diabetes es una enfermedad ampliamente extendida que afecta a todo rango de edades y miles de personas en el mundo dependen de ellos.
Artículo editado por Javier Sánchez.
Artículos que pueden interesarte
- Biorremediación: ¿Podemos usar organismos para descontaminar?
- Bacteriófagos: un candidato perfecto para combatir las bacterias multirresistentes
- Biofactorías. Los seres vivos en la producción industrial de biorreactores.
- La levadura como organismo modelo en investigación.
Bibliografía
How stem cells could fix type 1 diabetes (Liam Drew). Nature 595, S64-S66 (2021). doi: https://doi.org/10.1038/d41586-021-01842-x
Shapiro, A. M. J. et al. N Engl J Med. 2000 Jul 27;343(4):230-8. doi: https://doi.org/10.1056/NEJM200007273430401 PMID: 10911004.
D’Amour, K. A. et al. Nature Biotechnol. 24, 1392–1401 (2006). https://doi.org/10.1038/nbt1259
Karuranga S, Malanda B, Saeedi P, Salpea P. IDF Atlas 9th edition and other resources. Int Diabetes Fed 2019;9th editio:1–176






