¿Te suenan los conceptos de biofactorías o biorreactores? Todos los organismos cumplen una función en la naturaleza. Desde las bacterias, hasta los grandes depredadores, cada especie tiene su sitio. Durante miles de años, los humanos hemos aprovechado las características especiales de muchos de ellos para nuestro beneficio. Por ejemplo, la fermentación es una de estas «características» que aprovechamos de microorganismos como Saccharomyces cerevisiae… ¡Sigue leyendo para averiguar más!
Es evidente que nuestro conocimiento de estos distintos organismos ha ido en aumento. A día de hoy, grandes producciones industriales se basan en las capacidades de organismos concretos, y en nuestra habilidad para controlarlos.
Gracias a los avances en ingeniería genética, que nos permiten modificar, optimizar e introducir genes de unos organismos en otros, la industria de las biomoléculas (compuestos como grasas o proteínas, obtenidos a partir de los seres vivos) ha ido en aumento.
Hoy os hablaré de los organismos, microorganismos y de la ingeniería genética que hay detrás de muchas grandes producciones industriales. Innumerables biomoléculas casi imposibles de obtener hace unos años pueden ser producidas industrialmente en la actualidad. Todo ello gracias a las biofactorías.
Índice de contenido:
¿Qué son las biofactorías?

Si buscáis el término biofactoría en Google, es posible que encontréis este concepto asociado al tratamiento de aguas residuales. Pero en realidad, biofactoría es cualquier sistema de producción en el que la obtención del producto final requiera indispensablemente un organismo vivo para su elaboración. Teniendo esto en cuenta, el concepto puede extenderse a la producción de vino, cerveza, u otras comidas y bebidas que requieran cierta actividad microbiana como la fermentación. Hoy en día podemos transformar, modificar y controlar muchos otros organismos, como las levaduras, plantas e incluso células animales. Todo ello gracias a la ingeniería genética, lo que ha supuesto un auténtico boom en la industria de las biofactorías.
Como es evidente, cada organismo tiene unas características. Por ejemplo, la levadura es muy interesante por sus altas tasas de fermentación. Transforma azúcares en alcohol, lo que la hace ideal para la producción de bebidas fermentadas (vinos, cervezas, etc.). Otras, como por ejemplo bacterias del género Lactobacillus, se utilizan por su capacidad para producir ácido láctico, esencial para la fabricación de yogures o queso. ¡Pero hay mucho, mucho más!
La industria de las biomoléculas

Muchos seres vivos producen unos compuestos de gran interés llamados biomoléculas, como son las vitaminas, proteínas o grasas, que pueden tener una amplia gama de propiedades. Por ejemplo, algunas especies vegetales producen aceites esenciales increíblemente demandados por la industria de los perfumes. Otras, como el eucalipto o algunas plantas aromáticas, producen compuestos antibióticos y antifúngicos muy interesantes desde el punto de vista farmacológico.
Sin embargo, podrás imaginar que no es fácil producir cantidades industriales de muchas de estas biomoléculas. Un gran ejemplo es el taxol, un interesante compuesto anticancerígeno que proviene del tejo, Taxus ssp. En la naturaleza, la producción de esta molécula tan interesante se da en cantidades muy pequeñas, lo que requeriría de toneladas de árboles para producir tan sólo gramos de taxol. ¿Qué soluciones se han encontrado a este problema?
- Cultivos de células de tejo en suspensión. Es posible extraer y cultivar células de tejo, haciéndolas crecer en biorreactores (de los que hablaremos a continuación). En estos entornos controlados, la producción de taxol puede maximizarse, sin recurrir a la tala indiscriminada de árboles.
- Cultivos de otros organismos capaces de producir taxol. Nuestros conocimientos sobre ingeniería genética hacen posible crear organismos que pueden producir esta biomolécula . Recientemente se ha conseguido originar una cepa de levadura con diversos genes de tejo que componen gran parte de la ruta biosintética del taxol, y que de hecho puede producir este fármaco.
Biorreactores
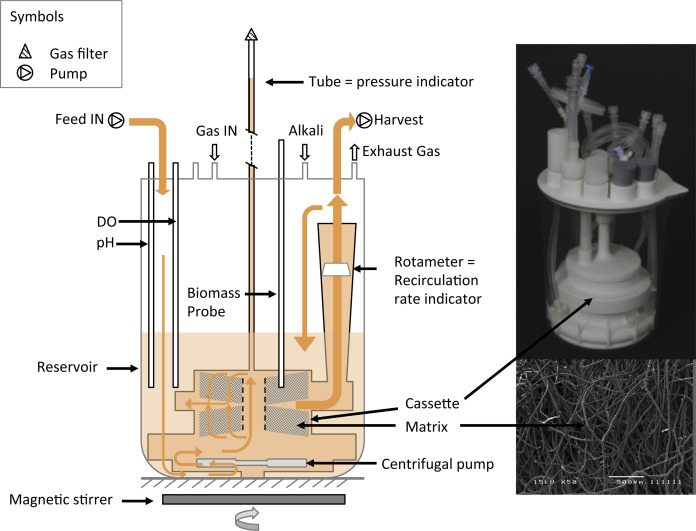
La base de una biofactoría es la posibilidad (realista) de producir algo (moléculas, proteínas, etc.) en gran escala gracias a un organismo vivo, y ello se consigue gracias a los biorreactores. Desde sencillos frascos estériles en agitación, hasta gigantescos barriles o tuberías infinitas, los biorreactores tienen muchas formas. Todos ellos con una característica común: deben mantener las condiciones ideales para que crezca el organismo que se está cultivando.
Un biorreactor debe ser estéril, de modo que sólo crezca el organismo de interés. Los modelos más modernos controlan todos los parámetros del medio de cultivo (pH, oxígeno, temperatura, agitación…) para que el organismo cultivado crezca de manera óptima. Muchos biorreactores incluso pueden descartar el medio y renovarlo según los nutrientes van siendo consumidos por el microorganismo cultivado, manteniendo un crecimiento continuo.

Los biorreactores se operan gracias a profesionales de dos ámbitos: tanto de la ingeniería química, para controlar el biorreactor y la operación en sí, como de la biología o biotecnología, que conozcan y manejen al organismo que se está cultivando. De este modo, las biofactorías implican necesariamente cierto nivel de multidisciplinariedad.
Es importante saber que un biorreactor no puede funcionar indeterminadamente. Con el tiempo, el organismo consume nutrientes, libera desechos, o incluso puede acumular mutaciones nocivas que hacen que el producto no sea adecuado. Por ello, cada cierto tiempo debe pararse la producción, esterilizar el reactor, y comenzar de nuevo. Las producciones más caras incluyen series de biorreactores, de modo que si uno tiene que parar, otros pueden seguir funcionando, de modo que la producción jamás cesa.
Proteínas y otros productos
Otros productos muy demandados por la industria médica son productos o fármacos de base proteica, como anticuerpos y hormonas. Como no podría ser de otro modo, esto incluye vacunas, interferones, anticuerpos y demás compuestos que pueden ser expresados y sintetizados a partir de genes.
Sin embargo, no todo vale, y no cualquier organismo puede producir un producto con unas características farmacológicas óptimas. Veremos tres ejemplos claros en tres organismos muy distintos: la insulina, la vacuna contra el ébola, y el interferón gamma.
1. Insulina
La insulina no es sino una proteína de unos 51 aminoácidos que secreta el páncreas y que permite el aprovechamiento metabólico de glúcidos. Los pacientes de diabetes tipo 1 no secretan esta hormona, por lo que su administración es indispensable para el tratamiento de esta enfermedad. No obstante, no es fácil encontrarla. Antiguamente, se obtenía insulina de cerdos que debían ser sacrificados. Gracias a los avances de la ingeniería genética, se consiguió que la bacteria Escherichia coli lograra producirla. Estas bacterias contenían en un plásmido los genes con la información para producir esta proteína. Así pudieron comenzar a explotarse industrialmente estas bacterias para obtener la hormona de una manera más sencilla y en grandes cantidades.
2. Vacuna contra el ébola

El ébola, un virus altamente peligroso, tuvo un foco mediático en 2014 al tenerse noticias de algunos casos en Occidente. Sigue siendo un virus altamente contagioso y prácticamente mortal en muchas zonas de África. En 2014 se obtuvieron patentes para producir un tratamiento contra este virus en la planta del tabaco, Nicotiana tabaccum, recurriendo de nuevo a la ingeniería genética. De este modo, se lograron plantas capaces de expresar anticuerpos contra el ébola. La vacuna, denominada ZMapp, no era sino un cocktail de distintos anticuerpos contra el virus, todos ellos producidos y expresados por distintas líneas de tabaco. En este caso, las facilidades de cultivar plantas, y no microorganismos, implicaban una reducción en los costes de producción.
3. Interferón Gamma
El Interferón Gamma (IFN-γ) es una molécula (citocina) muy importante para el funcionamiento del sistema inmunitario. Principalmente se utiliza para optimizar la respuesta inmune de pacientes, por ejemplo contra infecciones bacterianas y víricas graves. De manera puntual, se ha utilizado en el tratamiento de tumores, con el objetivo de activar la respuesta inmune innata y dificultar la irrigación sanguínea al tejido tumoral, lo que conduce a la muerte celular programada.
Para la producción de interferón gamma no basta con la síntesis de la proteína, sino que ésta debe ser modificada posteriormente. Las modificaciones postraduccionales son reacciones químicas (oxidación, glucosidación, etc.) que no cambian la estructura de la proteína, pero sí sus funcionalidades. Y lo más importante es que las modificaciones que llevan a cabo las células humanas no son las mismas que llevan a cabo otros organismos.
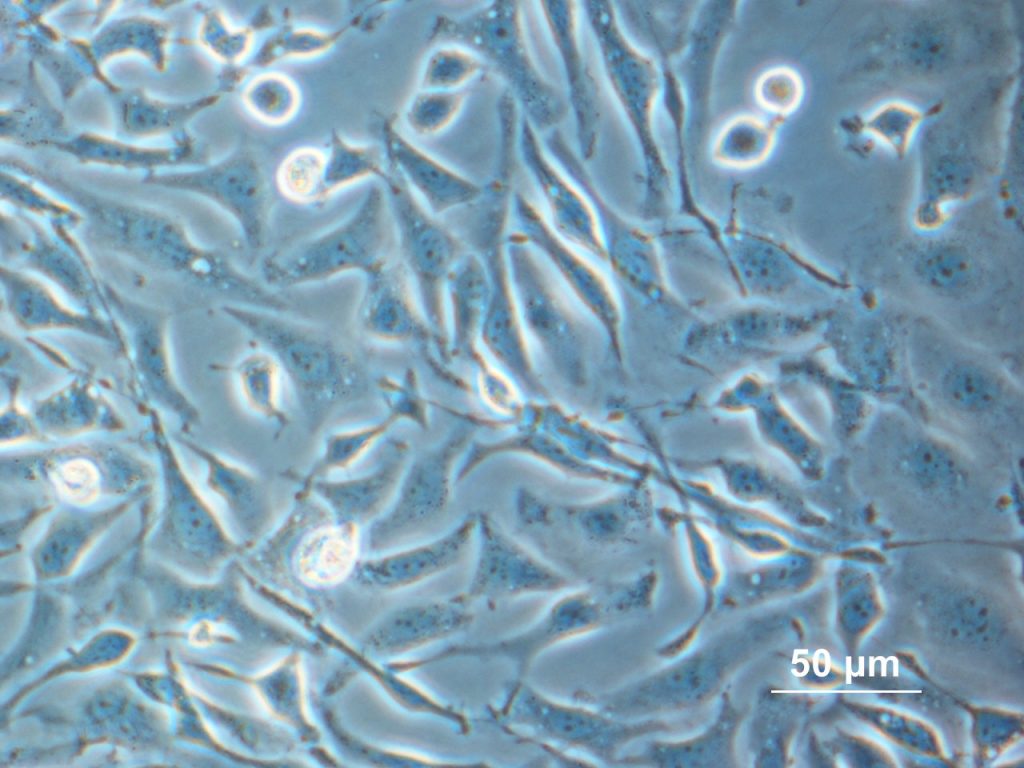
Por esto, inicialmente se recurrió a las Células de ovario de hámster chino (CHO) para su fabricación. Son fáciles de cultivar en biorreactores y llevan a cabo modificaciones muy similares a las humanas. Así, el interferón que producen es similar y seguro para su administración en humanos.
Con el avance de la ingeniería genética se ha conseguido que bacterias puedan producir un interferón similar al de humanos. Actualmente se utilizan bacterias humanizadas, capaces de llevar a cabo ciertas modificaciones en la proteína, que dan como resultado un producto farmacológicamente bueno. El uso de bacterias es preferible respecto a células animales, ya que tienen mayores tasas de crecimiento, de síntesis proteica y requieren condiciones de cultivo menos estrictas.
Otros procesos: La biorremediación
Las biofactorías y los biorreactores no sólo se emplean para producir compuestos, sino también para otras aplicaciones. Numerosos proyectos a nivel europeo y mundial están luchando por utilizar organismos para limpiar. Muchas bacterias son capaces de crecer y descontaminar suelos de metales pesados. De hecho, se usan habitualmente para limpiar escapes de petróleo como en el caso Prestige. Las plantas también pueden absorber contaminantes por sus raíces y retenerlos, impidiendo que se dispersen en el terreno.
Las plantas depuradoras de aguas son un claro ejemplo de biorremediación. En ellas existen auténticos biorreactores que contienen no una, sino cientos de especies de microorganismos capaces de limpiar el agua de materia orgánica y compuestos. Esto permite que el agua residual de las ciudades pueda ser tratada, descontaminada, y redirigida.

¿Qué nos depara el futuro?
La industria de las biofactorías está en auge, ya que permite una explotación de biomoléculas muy valoradas de forma relativamente sencilla y estandarizada. Al aumentar los avances en ingeniería genética, es posible que cada vez más compuestos difíciles de producir consigan crearse de forma industrial. Esto abarataría sus costes y pondría dicho producto al alcance de más personas.
No obstante, la industria basada en la ingeniería genética está muy regulada. En Europa es extremadamente difícil conseguir permisos para hacer explotaciones de organismos genéticamente modificados (OGM), mientras que en otros países como América lo tienen mucho más fácil. Es importante recordar que estos organismos, como es el caso de las bacterias productoras de insulina, pueden salvar vidas.
¿Y tú? ¿Conocías las biofactorías? Los organismos, y especialmente los microorganismos, son increíblemente flexibles; pueden producir desde cerveza hasta proteínas de alta calidad. ¿Ya sabías de alguna de estas capacidades? ¡Coméntanoslo!
Artículos que pueden interesarte
- ¿Cómo se descubre la causa genética de una patología?
- Ribosomas saltándose los stops: readthrough
- Las mutaciones silenciosas: ¿Cómo se generan las proteínas y qué efecto pueden tener sobre ellas?
- Almacenamiento de datos ¿Es el ADN el futuro?
Referencias
- Sonia Malik, Rosa M. Cusidó, Mohammad Hossein Mirjalili, Elisabeth Moyano, Javier Palazón, Mercedes Bonfill. Production of the anticancer drug taxol in Taxus baccata suspension cultures: A review. Process Biochemistry, 2011, 46 (1): 23-34.
- JingHong M Dejong, Yule Liu, Arthur P Bollon, Robert M Long, Stefan Jennewein, David Williams, Rodney B Croteau. Genetic engineering of taxol biosynthetic genes in Saccharomyces cerevisiae. Biotechnology bioengineering, 2006, 93(2): 212-2.
- Nabih A Baeshen, Mohammed N Baeshen, Abdullah Sheikh, Roop S Bora, Mohamed Morsi M Ahmed,Hassan A I Ramadan, Kulvinder Singh Saini, and Elrashdy M Redwan. Cell factories for insulin production. Microbiological Cell Factory, 2014, 13(141): 22-49.
- Qiang Chen & Keith R. Davis. The potential of plants as a system for the development and production of human biologics. 2016 (BioRxiv).







