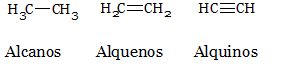Querido lector aunque suene demasiado poético, si alguno de tus amores: es el amor por la vida, por la naturaleza, a los seres vivos, por los placeres de la vida, a ti mismo, amor a tus seres queridos…sin darte cuenta; a lo que también estás amando es a la química orgánica.
Si no lo has pensado, nunca te has percatado o simplemente no has buscado interés en tal cosa te hago una pregunta retórica: ¿qué curioso que la hormona de la felicidad esté relacionada con la oxitocina, hormona también conocida como la del amor?
Índice de contenido:
Origen de la química orgánica
A comienzos del sigo XIX, los científicos clasificaron todos los compuestos conocidos en dos categorías: los compuestos orgánicos, derivados de los organismos vivos (plantas y animales) y los compuestos inorgánicos derivados de fuentes no vivientes (minerales y gases).
En 1828, a raíz de la síntesis propuesta por Friedrich Wöhler; la conversión de cianato de amonio (una sal inorgánica) en urea, compuesto orgánico que se encuentra en la urea, el término vitalismo comenzó a tener un cierto rechazado. Este término se empleó para explicar el porqué los compuestos orgánicos presentaban distintas propiedades con respecto a los compuestos inorgánicos.
En unas pocas décadas siguientes surgieron nuevas definiciones. Específicamente, los compuestos orgánicos se definieron como aquellos que contienen átomos de carbono, mientras que los compuestos inorgánicos se definieron como aquellos que carecen de dichos átomos.
La química orgánica está presente en todo lo que nos rodea: los alimentos que ingerimos, la vestimenta, medicamentos, olores, plaguicidas, pinturas, plásticos… hasta nosotros mismos somos un mar de complejas moléculas orgánicas: ADN, ARN, proteínas, ácidos grasos, azúcares etc. Por ello, con este post vamos a intentar acercar este mundo: el de la química orgánica a nuestro día a día.
La química de los compuestos más simples
El primer grupo funcional que se estudia desde la ESO son los alcanos y cicloalcanos. Compuestos pertenecientes a una clase aún mayor denominada hidrocarburos, también destacan los alquenos, alquinos y compuestos aromáticos. Los hidrocarburos son compuestos solamente formados por átomos de C y H.
La principal distinción entre los distintos compuestos son los enlaces que hay presentes en la molécula (Figura 1). Los hidrocarburos que no presentan enlaces pi, por lo que sólo presentan enlaces sigma, son los hidrocarburos saturados o alcanos. Los alquenos presentan un enlace sigma y otro enlace pi, lo que conlleva a que la molécula tenga un doble enlace; mientras que los alquinos presentan un triple enlace del resultado de un enlace sigma y dos enlace pi.
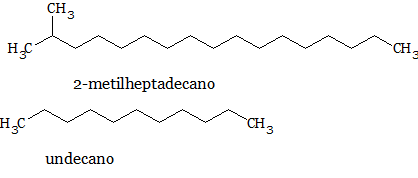
En nuestro día a día le debemos mucho a los hidrocarburos ya que gracias a ellos tenemos energía porque son derivados de combustibles fósiles, como el petróleo y gas natural. No obstante, los alcanos también aparecen en seres vivos y juegan un rol importante. Por ejemplo las feromonas, que son sustancias químicas que los insectos las utilizan como principal medio de comunicación; el 2-metilheptadecano, una feromona sexual usada por algunas polillas; y, el undecano, una feromona de agregación de algunas cucarachas (Figura 2).
Para alquenos también existen moléculas que nos afectan de primera mano, como por ejemplo el etileno (H2C=CH2). Esta sustancia a temperatura ambiente es un gas que actúa como hormona de crecimiento y desencadena el proceso de maduración. Este proceso afecta a la maduración de las frutas, por ejemplo, por lo que recuerda siempre separar la fruta más madura del resto, ya que es una fuente rica de gas etileno.
Los dobles enlaces también están muy presentes en la alimentación, más específicamente en los lípidos. Los triglicéridos son una clase principal de lípidos, aquellos triglicéridos que contienen dobles enlaces presentan un punto de fusión menor lo que hace que sea aceites (líquidos a temperatura ambiente), mientras que las cadenas saturadas (sin dobles enlaces) de triglicéridos son sólidos y se denominan grasas (Figura 3). De ahí que la comida rápida sea perjudicial para la salud ya que una elevada concentración de grasas saturadas puede producir enfermedades.
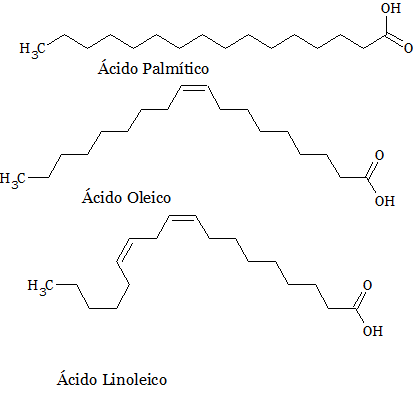
Estos ácidos grasos son los que están presentes en la bellota y aceita de oliva con una proporción muy similar, siendo el ácido oleico, el ácido graso que se encuentra líquido en los jamones ibéricos.
Dentro de los numerosos ejemplos que se pueden añadir queremos finalizar este bloque de hidrocarburos haciendo referencia a los alquinos y compuestos aromáticos. Un ejemplo de esto sería la selegilina, un compuesto recetado en combinación con L-Dopa en la enfermedad del Parkinson. Tanto el triple enlace como el anillo becénico le otorga a la molécula una elevada rigidez estructural, permitiéndole así unirse selectivamente a la enzima monoamina oxidasa B y como consecuencia reducir la producción dopamina en el cerebro.
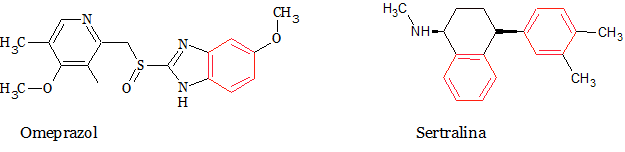
Los compuestos aromáticos, cuya estructura más básica es el benceno que tuvo un origen y un descubrimiento cuanto más curioso, están presentes en numerosos fármacos comerciales (figura 4). El omeprazol, inhibidor de la bomba de protones usado en el tratamiento de las úlceras y el reflujo gástrico y la sertralina usado para la depresión.
Los átomos de oxígeno en la química orgánica
Existe un espectro variado de grupos funcionales que contienen átomos de oxígeno ya que puede estar enlazado al átomo de carbono, teniendo una amplia variedad: alcoholes, cetonas, aldehídos, éteres, ácido carboxílico. Por si fuera poco, el átomo de oxígeno se puede encontrar formando compuestos enlazados a otros elementos como el azufre, fósforo, nitrógeno…es realmente para volverse loco.
En este post se citarán ejemplos de grupos funcionales donde el átomo de oxígeno se encuentre enlazado con enlace simple o doble a átomos de carbono. El enlace simple se forma en los alcoholes mientras que en los otros grupos se forma el doble enlace dando lugar a los grupos carbonilos. En mi primer artículo ya se hablaba sobre los alcoholes, explicando además el uso de reacciones de oxidación presentes en nuestro día a día.
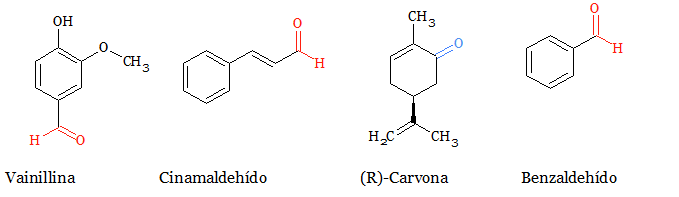
Las cetonas (R2CO) y aldehídos (RCHO) son similares en cuanto a su estructura, como ya hemos dicho, ambos están tienen presente un grupo carbonilo (C=O). El grupo carbonilo de un aldehído está flanqueado por un átomo de hidrógeno, mientras que el de una cetona lo está por dos átomos de carbón. Los aldehídos y cetonas determinan mucho de los sabores que se reconocen con facilidad en nuestro día a día: Vainilina (aroma a vainilla), Cinamaldehído (aroma a canela), (R)-Carvona (aroma a menta) y Benzaldehído (aroma a almendras) (Figura 5).
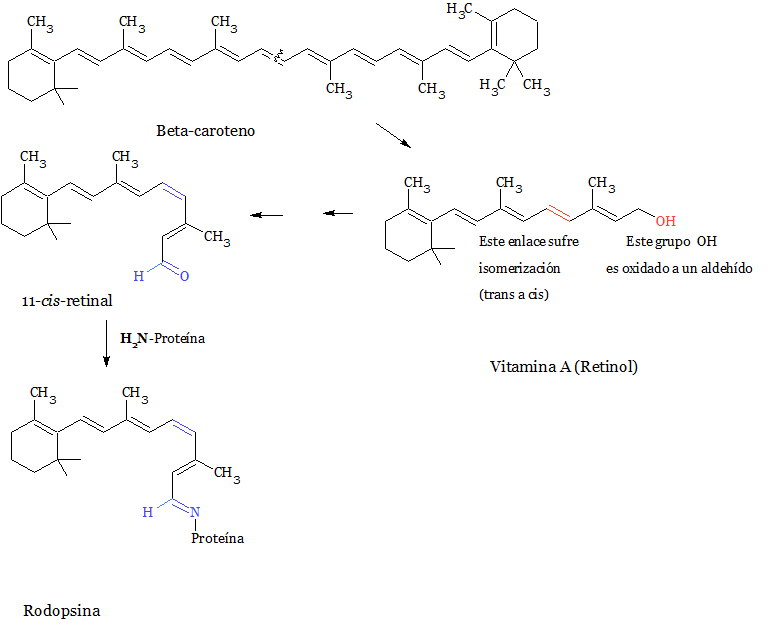
Un proceso bioquímico (Figura 6) que es realmente importante ya que, gracias a éste, el cerebro detecta dicha molécula y lo interpreta como visión. Este proceso es la degradación del beta-caroteno para dar lugar a la vitamina A (también conocido como retinol, un alcohol).
El beta caroteno es un terpenoide sintetizado a partir de ocho unidades de isoprenos que se encuentra en frutas y verduras otorgando a dichos alimentos un color anaranjado, como en las zanahorias. Éste se metaboliza en el hígado dando lugar a la vitamina A, que sufre una reacción de oxidación e isomerización para dar lugar a un compuesto que contiene un aldehído.
El aldehído resultante reacciona con un grupo amino de una proteína llamada opsina dando lugar a la rodopsina. Esta molécula es capaz de absorber un fotón de luz y sufrir un proceso de fotoisomerización (de un doble enlace cis a un doble enlace trans); siendo este cambio el que es captado por nuestro cerebro e interpretado como visión. La deficiencia por lo tanto, de la vitamina A puede conducir a ceguera nocturna.
La química orgánica, presente hasta en las proteínas
Por último, de la inmensa variedad de grupos funcionales y posibilidades que existen en la química orgánica, quiero destacar entre todos dos grupos funcionales: los compuestos con ácidos carboxílicos y compuestos que presentan átomos de nitrógeno ¿Por qué? Las proteínas son polímeros naturales que se ensamblan a partir de monómeros de aminoácidos a través de enlaces peptídicos, como si fuera un rompecabezas. Los aminoácidos están formados por un grupo amino (NH2) y un grupo carboxilo (COOH), siendo estos dos grupos los responsables del enlace peptídico. Existen un total de 20 aminoácidos que están presentes en la naturaleza formando proteínas.
Los aminoácidos (a excepción de la glicina), al igual que otros compuestos, pueden existir en dos formas simétricas del mismo modo que la mano derecha e izquierda, es decir, son imágenes especulares que no se pueden superponer, por lo que se les llama moléculas quirales. Estos compuestos especulares o enantiómeros se denominan L y D (del latín levo y dextro), lo curioso de todo esto, es que las proteínas tienen todos los aminoácidos de tipo L, mientras que los azúcares de los ácidos nucleicos son de tipo D. Si no fuera así, ni proteínas ni azúcares tendrían la estructura adecuada para cumplir su misión.
Como se pueden imaginar queridos lectores si los aminoácidos forman proteínas, éstos pueden estar presentes en numerosos ejemplos cotidianos, alimentación, medicamentos etc. Quiero compartir uno realmente interesante y que creo que os puede resultar bello.
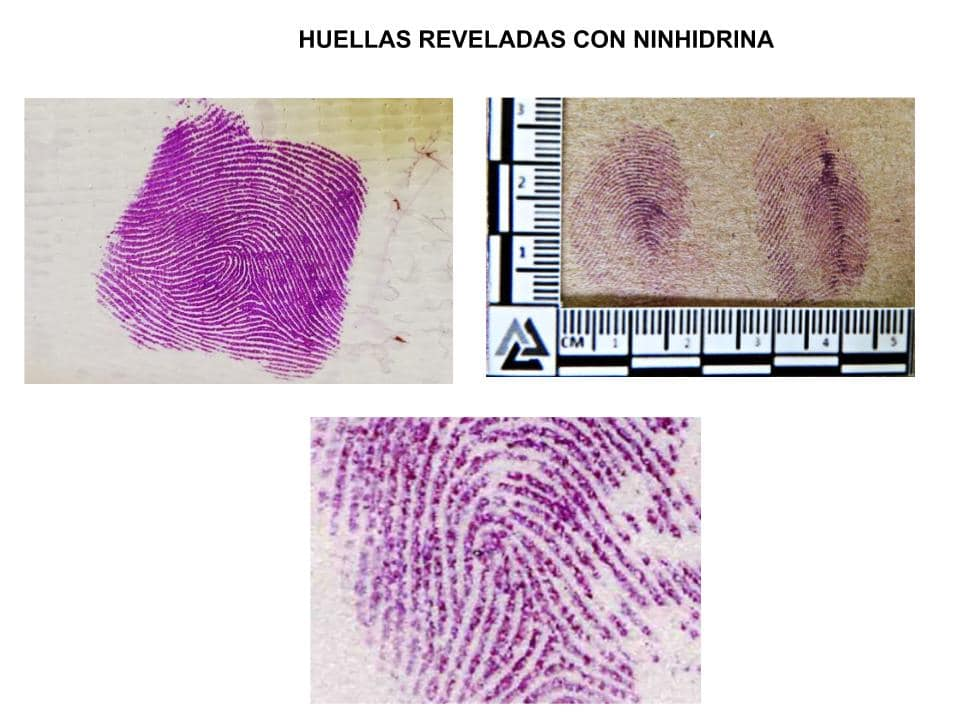
¿Cómo se puede explicar la detección de las huellas digitales desde el punto de vista químico? Las huellas digitales se crean por los restos de sudor encontrados en la superficie de la piel. La composición es 99% agua y en ese 1% existe una variedad de compuestos orgánicos, que incluyen los aminoácidos. Éstos están presentes en concentraciones muy pequeñas pero son relativamente estables durante largos períodos. Al tratarse con ninhidrinas, se produce una reacción entre ambos compuestos y se forma una imagen fluorescente (Figura 7). Para obtener mejores resultados, dicha solución se aplica en la oscuridad y a temperatura ambiente.
Conclusión
Imagino que como ya te habrás dado cuenta, la química orgánica está presente en nuestro día a día por donde quiera que mires. En este post se han visto ejemplos de compuestos que están presentes en los seres vivos como las feromonas. Moléculas de largas cadenas presentes en la alimentación. Estructuras complejas con variedad de grupos funcionales en los medicamentos, reacciones químicas que ocurren en todo momento y te permiten que puedas ver y leer dicho artículo y aplicaciones prácticas de la química orgánica.
Sí que es cierto que te podrás preguntar, ¿para que yo quiero saber todo esto?, pero imagino que si has llegado hasta el final del artículo, es porque te interesa, te apasiona el conocer las cosas que nos rodean y eres seguidor a la frase de que «el conocimiento no ocupa lugar». Este mundo es fascinante y realmente bello, simplemente hay que observarlo con los ojos del conocimiento que nos proporciona la ciencia.
¿Te apasiona la industria química y ves que puedes impulsar tu carrera profesional en este sector? Nuestro compañeros de STEM Future Education ofrecen distintas formaciones entre los que se encuentran el Máster de Acceso a la Industria Química.
Bibliografía
Klein D., (2008) Química Orgánica, Editorial medica Panamericana.