Fue uno de los primeros principios activos usados para tratar tumores de tipo hormonal y hoy en día es uno de los tratamientos más utilizados en cáncer de mama. La historia detrás del desarrollo de este fármaco es particular, ya que a pesar de su éxito, no consiguió los resultados esperados inicialmente.
Hablamos del tamoxifeno, cuyo proyecto comenzó como una búsqueda de una píldora anticonceptiva y acabó obteniéndose un anticancerígeno contra el cáncer de mama. ¿Por qué se produjo este giro en la investigación? ¿Por qué ha sido tan importante como tratamiento del cáncer de mama? La investigación estuvo a punto de frenarse antes de su aprobación como tratamiento en cáncer de mama en 1977, lo que hubiera provocado que este principio activo nunca saliera a la luz.
Índice de contenido:
El descubrimiento de un anticancerígeno en la búsqueda de un anticonceptivo
La historia comienza en los años 30, cuando se relacionaron por primera vez los estrógenos y el cáncer de mama. Con este descubrimiento, las principales compañías farmacéuticas se enfocaron en investigar y examinar compuestos similares a las hormonas estrogénicas. Esto llevó a Dorothy Crowfoot a descubrir una estructura química que serviría como base para sintetizar compuestos similares al estrógeno: el trifeniletileno.
En base a esta estructura, la compañía farmacéutica ICI (ya inexistente hoy en día) comenzó con dos proyectos, liderados ambos por el doctor Arthur Walpole: uno principal, con el objetivo de obtener una píldora anticonceptiva oral (una «pastilla del día después»); y otro secundario, buscando la aplicación de estas estructuras en el tratamiento de los cánceres de tipo hormonal, principalmente cáncer de mama.
Con estos objetivos, fue en 1962 cuando se sintetizó el compuesto ICI 46,474 (posteriormente denominado tamoxifeno) gracias al trabajo del nombrado Walpole junto a la química Dora Richardson y el biólogo Mike Harper. Este compuesto se probó en ensayos para evaluar su uso tanto en anticoncepción como en tratamiento del cáncer de mama, en los cuales se comprobó que la toxicidad y efectos adversos de este compuesto eran mucho menores a otros compuestos trifeniletilénicos, manteniendo su potencia.
Teniendo en cuenta las recientes complicaciones y controversia que habían aparecido tras el caso de la talidomida, prohibida en 1961 a raíz del nacimiento de niños con malformaciones por su administración durante el embarazo, los ensayos en el caso del tamoxifeno fueron exhaustivos, siendo el primer principio activo evaluado mediante test teratogénicos (pruebas para evaluar la seguridad durante el embarazo). En el artículo de Alberto Rivera Ramos publicado en Microbacterium puedes conocer un poco más los casos de algunos fármacos retirados, como la talidomida.
Resultados de ensayos practicados durante los años 60 probaron que el tamoxifeno no era un buen candidato para una píldora anticonceptiva, ya que en lugar de suprimir la ovulación como se pretendía, la estimulaba. A pesar de este fracaso, se observó también en un estudio en 1971 que el tamoxifeno provocaba represión tumoral en pacientes con cáncer de mama, sin producir grandes efectos adversos, lo que parecía garantizar una continuidad en la investigación de este compuesto como anticancerígeno.
Pero hay que tener en cuenta en qué época se dio este proceso. En los años 60 y 70 el mercado de un fármaco anticancerígeno se consideraba irrelevante, y así lo interpretó la farmacéutica ICI, que instó a Walpole, Richardson, Harper y al resto del equipo a frenar la investigación del tamoxifeno, ya que lo que estaban buscando era un anticonceptivo, que es lo que proporcionaría beneficio económico a la empresa. El motivo dado para detener el proyecto fue que el fármaco no amortizaría los costes de su desarrollo.
El mercado farmacéutico no tenía razón
Los resultados del compuesto como anticancerígeno fueron publicados, lo que provocó una presión de la sociedad científica hacia la compañía farmacéutica, que junto con la presión interna de los investigadores que formaban parte del proyecto, llevó a la compañía farmacéutica a reconsiderar su decisión y a abrir de nuevo el proyecto del tamoxifeno en 1973.
Así, y tras los ensayos clínicos pertinentes, el tamoxifeno fue aprobado en 1977 por la FDA (principal organismo farmacéutico de Estados Unidos). Años más tarde, a mediados de los 80, y gracias al trabajo de investigadores como Virgil Craig Jordan, este fármaco era ya un tratamiento de elección en cáncer de mama, y terminó por ayudar a salvar miles de vidas en todo el mundo.
Arthur Walpole murió en 1977, sin conseguir ver cómo el tamoxifeno llegó a ser un fármaco milagro para miles de pacientes de cáncer de mama, pero su insistencia, junto con la de sus colaboradores, en conseguir terminar con el desarrollo de este compuesto fue lo que provocó su comercialización, y en consecuencia su éxito como anticancerígeno.

¿Por qué es tan útil el tamoxifeno en cáncer de mama?
El tamoxifeno supuso un antes y un después en el tratamiento de cáncer de mama positivo para receptor de estrógenos y progestágenos (ER+/PR+), es decir, aquellos en los que la estimulación por estrógenos y progestágenos se relaciona con la aparición del tumor y su crecimiento descontrolado. En este tipo de cáncer de mama, desactivar la señalización estrogénica provoca que el tumor frene su crecimiento, lo que, unido a la quimioterapia, se ha comprobado que produce una disminución de la masa tumoral.
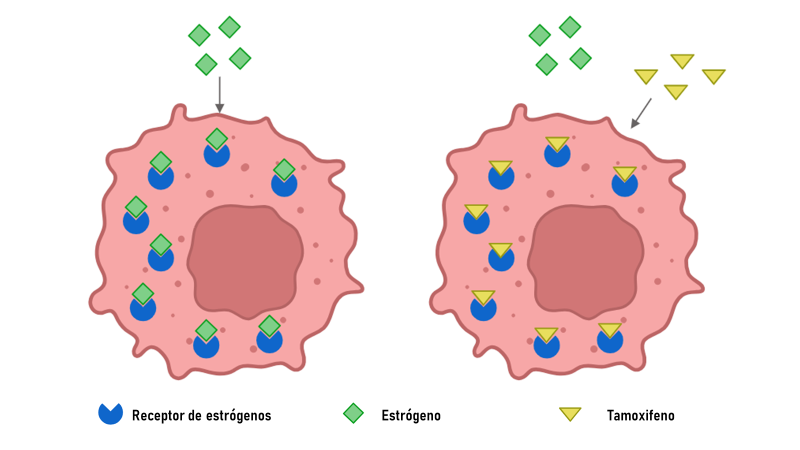
El tamoxifeno actúa bloqueando el receptor de estrógenos (Figura 3). La molécula se une al mismo receptor que los estrógenos, funcionando como agonista parcial, impidiendo que los estrógenos endógenos generados en el organismo se unan al receptor, ya que su sitio está ya ocupado por el tamoxifeno. Al no poder unirse los estrógenos no se podrá producir la señalización, y se impide la proliferación del tumor que sería causada por esta señalización. En definitiva, se frena el crecimiento del tumor.
Desde la aparición del tamoxifeno se ha seguido trabajando en conseguir otros tratamientos que modulen la señal de estrógenos y progestágenos. Es el caso de los inhibidores de la aromatasa (AI), la enzima que permite la síntesis de estradiol, uno de los pasos necesarios en la síntesis endógena de estrógenos. Estos compuestos, tales como exemestano, anastrozol o letrozol, impiden por tanto la síntesis de estrógenos endógenos, disminuyendo la proliferación y el desarrollo del tumor.
Pero el tamoxifeno no puede tratar todos los casos
Aproximadamente el 60% de los tumores de mama son ER+, por lo que el tamoxifeno ha podido usarse como tratamiento adyuvante en la mayoría de los casos de cáncer de mama. En aquellos tumores ER-, es decir, aquellos en los que la señalización estrogénica no está relacionada con el desarrollo del tumor, el tratamiento es más complejo, ya que el uso de moduladores estrogénicos no tiene efecto (Figura 4).
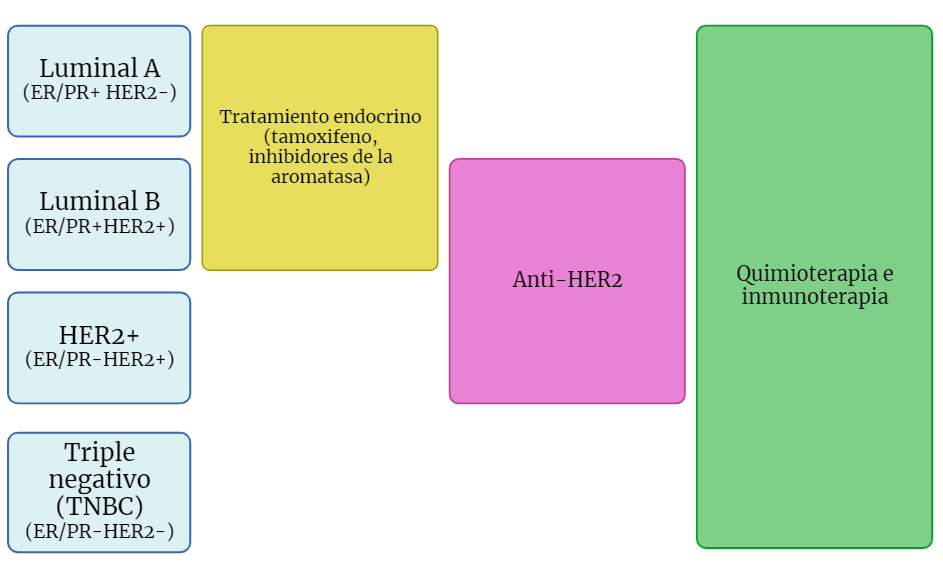
A pesar de ello, se han desarrollado nuevos tratamientos para cánceres ER- , y principios activos como trastuzumab o pertuzumab son de uso habitual en tumores ER- HER2+, en los que los receptores HER2 están implicados en el desarrollo del tumor.
Aquellos tumores en los que ni el receptor de estrógenos ni el receptor HER2 están implicados (ER- HER2-), denominados cáncer de mama triple negativo (TNBC, por sus siglas en inglés), son los de más difícil tratamiento, ya que el uso de los compuestos nombrados anteriormente no funciona para reducir ni frenar el tumor y las opciones de tratamiento pasan por la quimioterapia. Pese a ello, nuevos marcadores y por tanto nuevos tratamientos se encuentran en proceso de desarrollo, lo que puede mejorar el manejo de estos últimos casos.
Conclusión
La aparición del tamoxifeno supuso un «milagro» para muchas pacientes de cáncer de mama, tras comprobarse que su uso como adyuvante reduce de forma sustancial la proliferación y el crecimiento tumoral.
Si hubiera sido por el mercado y el negocio farmacéutico este compuesto no hubiera visto nunca la luz. Por esto los investigadores que presionaron para que la investigación científica superara al negocio deben ser nombrados (Walpole, Richardson o Harper). Ellos son realmente los culpables de que se optara por seguir con las pruebas científicas y clínicas y durante años se salvaran miles de vidas gracias al tamoxifeno, un fármaco que no consiguió lo esperado, pero que acabó ayudando a miles de pacientes. De hecho, Dora Richardson declaró posteriormente que recibió miles de cartas de pacientes tratadas con tamoxifeno en las que le agradecían su acción en la investigación.
Actualmente otros tratamientos complementan a los moduladores estrogénicos como el tamoxifeno, y con esfuerzo colectivo se ha conseguido una gran disminución en la mortalidad de pacientes con cáncer de mama en los últimos años, aunque se debe seguir trabajando para seguir mejorando las cifras.
Artículo editado por Ada Muñoz
Bibliografía
Cole, M P, Jones And, C T A, Todd, I D H. A NEW ANTI-OESTROGENIC AGENT IN LATE BREAST CANCER AN EARLY CLINICAL APPRAISAL OF IC146474. Br J Cancer. 1971. 25(2):270-5.
Craig Jordan, V. 50th anniversary of the first clinical trial with ICI 46,474 (tamoxifen): Then what happened?. Endocr Relat Cancer. 2021. 28(1): R11–R30. doi:10.1530/ERC-20-0335.
Quirke, V. Tamoxifen from failed contraceptive pill to best-selling breast cancer medicine: A case-study in pharmaceutical innovation. Front. Pharmacol. 8:620.doi: 10.3389/fphar.2017.00620.





