El incremento desmedido en los últimos años de enfermedades como la obesidad o la diabetes tipo 2, ha hecho que se disparen el uso de fármacos a modo de inyecciones para la pérdida de peso.
La obesidad se caracteriza por una acumulación excesiva de peso y grasa corporal, y es la causante de más de 5 millones de muertes anuales. La diabetes es definida como un desorden metabólico caracterizado por hiperglucemia crónica -niveles de glucosa en sangre elevados de forma constante-, y afecta a más de 500 millones de personas en todo el mundo.
La pérdida de peso y un buen control glucémico constituyen uno de los principales objetivos en ambas patologías. Por ello, en los últimos años se ha puesto el foco en un grupo de fármacos que son eficaces en ambos escenarios: los análogos del GLP-1 o ‘incretinmiméticos’.
Índice de contenido:
Concepto de incretina y un poco de fisiología
Estas inyecciones se basan en un tipo de hormonas que ejercen múltiples funciones en el organismo, por lo que, para comprender el por qué de su uso, primero debemos asentar algunos conceptos.
Las incretinas son hormonas intestinales que aumentan la secreción de insulina después de las comidas, lo que facilita que los niveles de glucosa en sangre vuelvan a valores normales. Esta situación fue descrita el siglo pasado, cuando se observó que una carga de glucosa oral incrementaba los niveles de insulina, mientras que una carga parenteral (sin pasar por el tubo digestivo) no lo hacía, fenómeno que hoy conocemos como ‘efecto incretina’.
Las dos incretinas más estudiadas son el polipéptido inhibidor gástrico (GIP) y el péptido análogo al glucagón tipo 1 (GLP-1), siendo esta última en la que nos centraremos mayoritariamente.
El GLP-1 se sintetiza y libera concretamente en las células L localizadas a lo largo del intestino delgado y grueso. Una vez liberado a la circulación, el GLP-1 se une a receptores específicos localizados en órganos como el páncreas, cerebro, corazón, riñones y a lo largo del tracto gastrointestinal, donde ejerce acciones específicas, como las indicadas en la siguiente figura.
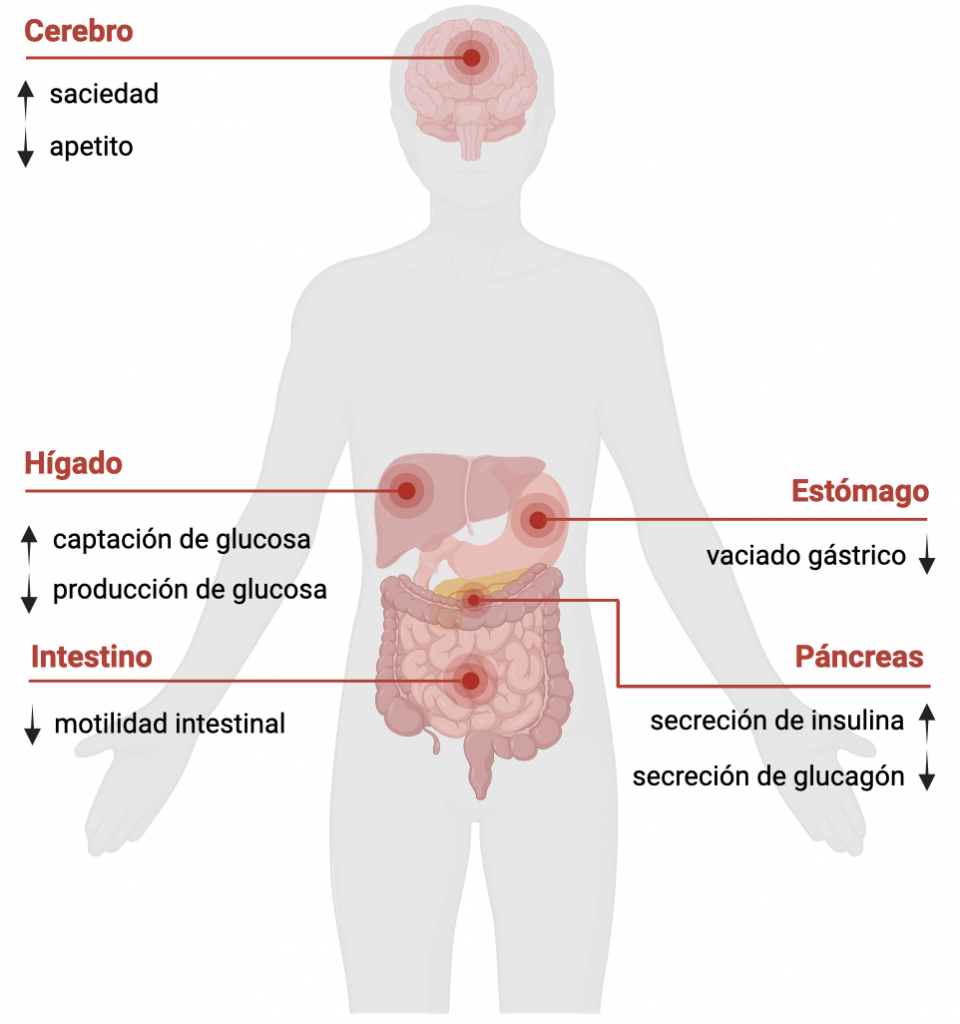
Imagen elaborada por Óscar Tovar Ferrero con BioRender.
Estas son sólo algunas de las muchas acciones del GLP-1, pero que sirven para comprender el por qué se han desarrollado fármacos que tratan de mimetizar o ‘imitar’ la acción de esta hormona para el tratamiento de la diabetes tipo 2 o la obesidad.
La particularidad de estos medicamentos es que son inyectables -como la insulina-, motivo por el cual muchos pacientes rehúsan el tratamiento con ellos. No obstante, en 2020 la Agencia Europea del Medicamento aprobó la comercialización de semaglutida (un análogo del GLP-1) en forma oral para el tratamiento de la diabetes tipo 2, lo que ha supuesto un gran avance en el tratamiento de estos pacientes.
Twincretinas: una nueva era
Hace escasos meses, varios medios de comunicación se hicieron eco de “un nuevo fármaco inyectable contra la obesidad que consigue adelgazar un 20%”. Así era el titular que medios como La Sexta publicaban para dar a conocer este medicamento: la tirzepatida.
El estudio al que hace referencia fue publicado en junio de 2022 en la revista The New England Journal of Medicine, donde se vio que tras 72 semanas de tratamiento se conseguían pérdidas de hasta un 22,5% del peso corporal.
Lo que hace especial a este nuevo fármaco es su capacidad para actuar sobre los receptores de GLP-1 y GIP. La activación de ambos receptores parece ejercer un efecto sinérgico, obteniendo así mayores reducciones de peso. Debido a este mecanismo de acción dual también se la conoce como ‘twincretina’, y en Estados Unidos ya está aprobada para el tratamiento de la diabetes tipo 2 y se está investigando también para el tratamiento de la obesidad, cuyos resultados parecen prometedores.
Nexo común
Actualmente, en España están comercializados los siguientes análogos del GLP-1: dulaglutida, exenatida, liraglutida, lixisenatida y semaglutida. Todos ellos tienen una cosa en común más allá del sufijo: deben prescribirse en combinación de ejercicio físico y alimentación saludable.
El estilo de vida juega un papel fundamental en el tratamiento de cualquier patología, pero en el caso de la obesidad y diabetes es imprescindible adquirir buenos hábitos lo antes posible, ya que únicamente con el fármaco no se alcanzarán los objetivos.
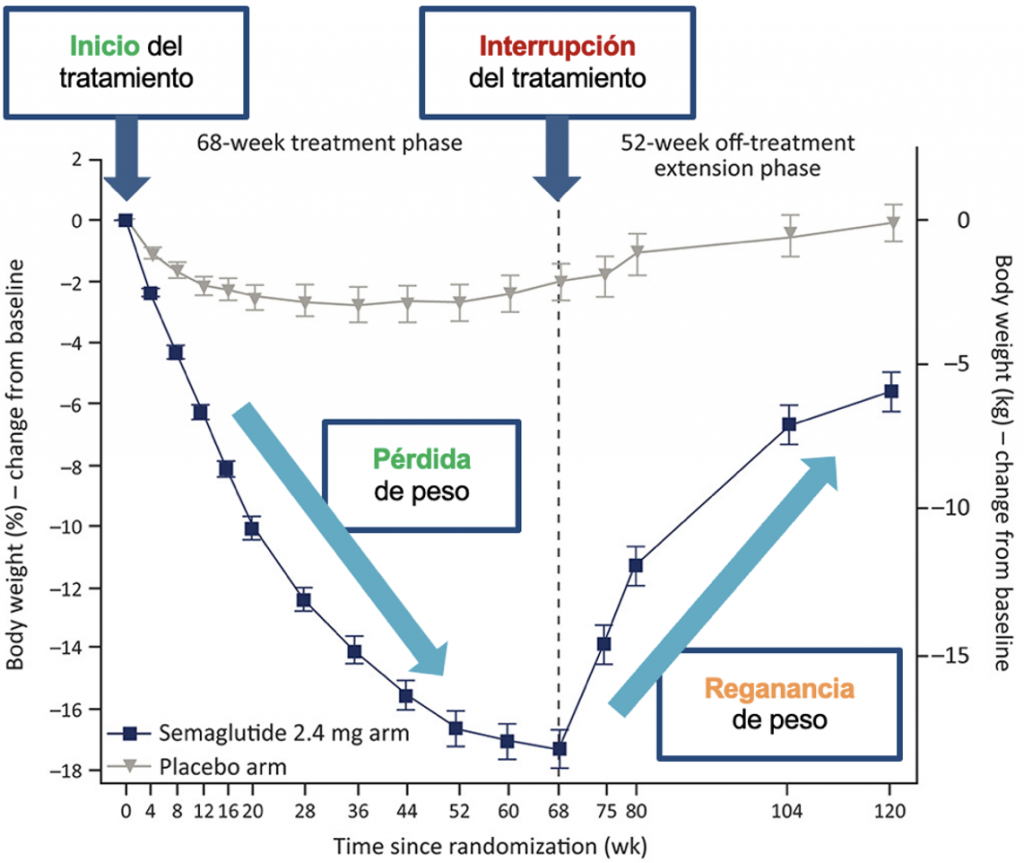
Como una imagen vale más que las mil palabras que ocupan este artículo, en el siguiente gráfico podemos ver lo que ocurre tras la interrupción del tratamiento con semaglutida después de 68 semanas de tratamiento.
Tal y como se puede observar en la imagen, la interrupción del tratamiento con semaglutida produjo inmediatamente un incremento posterior del peso corporal, lo que muestra que el tratamiento farmacológico puede ser de gran ayuda en el manejo del peso, pero la intervención y seguimiento de un estilo de vida saludable es fundamental para garantizar el éxito del tratamiento, tal y como muestran las guías clínicas de referencia.
Conclusiones
Como hemos visto, los resultados que ofrecen estas inyecciones para la pérdida de peso en pacientes con obesidad son realmente optimistas. No obstante, también hemos visto lo que ocurre cuando se interrumpe el tratamiento farmacológico y no se mantienen los hábitos de vida saludable adquiridos.
La ciencia avanza, y con ella el desarrollo de nuevas terapias y medicamentos que tratan de mejorar la calidad de vida de las personas, pero no podemos olvidar que la prevención debería ser siempre el objetivo prioritario.
Bibliografía
1. Sun H, Saeedi P, Karuranga S, et al. IDF Diabetes Atlas: Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045. Diabetes Res Clin Pract. 2022;183:109119.
2. Campbell JE, Drucker DJ. Pharmacology, physiology, and mechanisms of incretin hormone action. Cell Metab. 2013;17(6):819-837.
3. Nauck MA, Quast DR, Wefers J, Pfeiffer AFH. The evolving story of incretins (GIP and GLP-1) in metabolic and cardiovascular disease: A pathophysiological update. Diabetes Obes Metab. 2021;23 Suppl 3:5-29.
4. Min T, Bain SC. The Role of Tirzepatide, Dual GIP and GLP-1 Receptor Agonist, in the Management of Type 2 Diabetes: The SURPASS Clinical Trials. Diabetes Ther. 2021;12(1):143-157.
5. European Medicines Agency. Science medicines health. Rybelsus – Semaglutide. https://www.ema.europa.eu/en/medicines/human/EPAR/rybelsus#authoris
6. Jastreboff AM, Aronne LJ, Ahmad NN, et al. Tirzepatide Once Weekly for the Treatment of Obesity. N Engl J Med. 2022;387(3):205-216.
7. Wilding JPH, Batterham RL, Davies M, et al. Weight regain and cardiometabolic effects after withdrawal of semaglutide: The STEP 1 trial extension. Diabetes Obes Metab. 2022;24(8):1553-1564.