Las terapias génicas son, desde hace ya un tiempo, una realidad en la clínica y cada vez van ampliando más su aplicabilidad a todo tipo de enfermedades y trastornos. Uno de los últimos avances relacionados con este tipo de terapias es la restauración de la audición en personas con pérdida de la audición congénita.
Pero, a pesar de que escuchamos y vemos numerosas noticias como esta referentes a terapias génicas, ¿sabemos exactamente en qué consisten y cuál es su objetivo?
Si quieres saber algo más sobre las terapias génicas en general, y más concretamente sobre los últimos tratamientos desarrollados destinados a tratar la pérdida de audición no te pierdas este post.
Índice de contenido:
¿Qué son las terapias génicas?
Para comenzar es necesario comprender qué es una terapia génica y qué objetivo tienen estas terapias. Con una terapia génica se pretende corregir genéticamente la causa de una enfermedad, recuperando o reprimiendo la expresión de un gen en función de si su expresión es beneficiosa o perjudicial en el desarrollo de la enfermedad.
Este tipo de terapias son muy útiles sobre todo cuando hablamos de enfermedades monogénicas. En este tipo de enfermedades la alteración de un único gen es la causa principal de la enfermedad, al contrario que en las multigénicas en las que alteraciones en varios genes causan la aparición de la enfermedad. Al ser un único gen el que se debe corregir será mucho más sencillo dirigir y diseñar la terapia génica.
Revertir genéticamente el problema que causa la enfermedad se puede llevar a cabo de dos formas principalmente: las terapias génicas de transferencia de genes o las terapias génicas destinadas a editar el genoma.
En el primer tipo lo que se trata de hacer es introducir en la célula una copia funcional de un gen alterado para que pueda producirse la proteína que no se estaba produciendo correctamente, o introducir una copia de un gen que codifique para una proteína que reprima la función de otra que está causando el trastorno. En definitiva, se introduce nuevo material genético en la célula para que este sea usado para combatir la enfermedad.
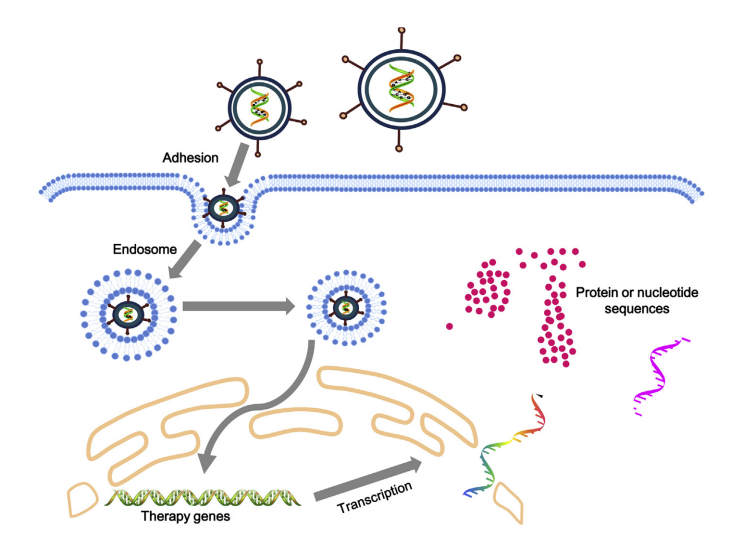
La edición del genoma, sin embargo, no consiste en introducir material genético nuevo para sustituir algo que no funciona, sino que se trata de arreglar lo que está mal, editándolo. Para ello se introducen herramientas en la célula capaces de editar el genoma, como son las herramientas CRISPR-Cas. Este artículo informa precisamente sobre la primera terapia génica basada en estas herramientas.
La introducción de estos nuevos elementos, ya sea material genético nuevo o herramientas que permitan editar el ya existente no se puede realizar, generalmente, de forma directa. Se necesita un vector en el que empaquetar el material genético que se pretende introducir y que sea capaz de llevarlo al interior de la célula de tal forma que esta lo pueda utilizar después en su beneficio.
Para ello se utilizan en muchos casos vectores virales, ya que los virus son capaces de llevar su material genético al núcleo celular, de tal forma que la información introducida podrá ser utilizada fácilmente por la célula. Entre ellos destacan los lentivirus o, como veremos más adelante en el caso de las terapias génicas destinadas a restaurar la audición, los adenovirus.
La otoferlina: clave en la audición y en el desarrollo de las nuevas terapias
Centrándonos ya en la noticia que motiva este artículo, las terapias génicas publicadas capaces de mejorar la audición en casos de sordera hereditaria tienen como objetivo reestablecer la función de una proteína clave para la audición, la otoferlina.
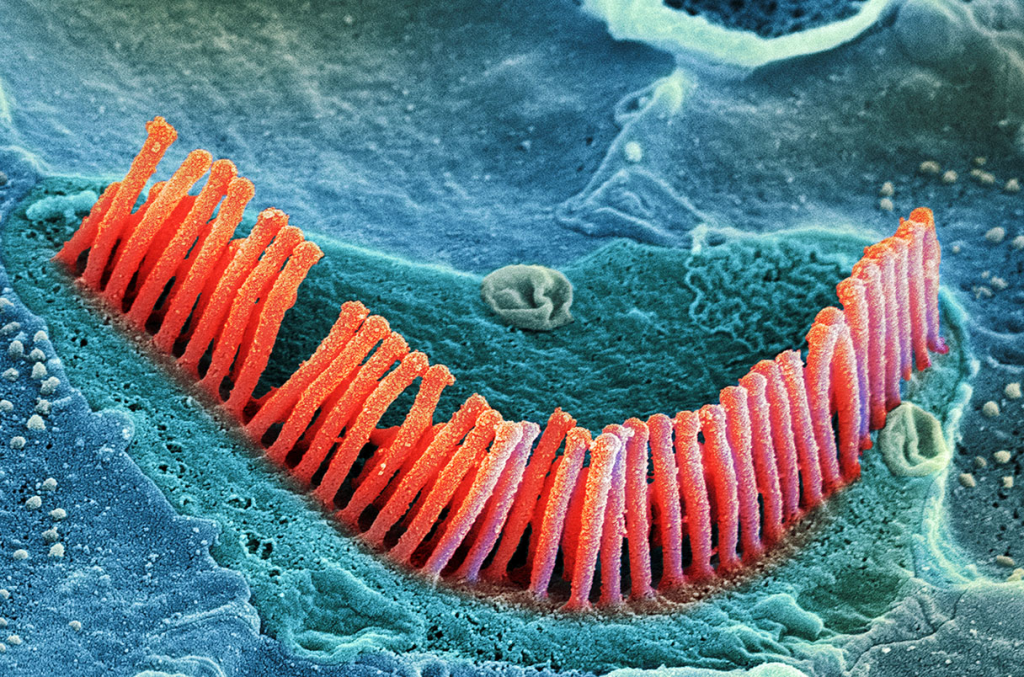
La otoferlina es una proteína codificada por el gen OTOF y que actúa en las células ciliadas del oído interno, ubicadas en la cóclea. Básicamente interviene en el proceso mediante el cual un sonido se transforma en una señal eléctrica para que nuestro cerebro lo pueda procesar.
En concreto, la otoferlina es clave en la transmisión de la señal de calcio implicada en la sinapsis glutamatérgica entre las células ciliadas y las fibras nerviosas del nervio auditivo. Cuando existe una mutación en el gen OTOF que provoca que la proteína no sea funcional o no se pueda producir, esta sinapsis no se producirá correctamente. Si esto ocurre, la señal nerviosa que debería producirse a consecuencia de un sonido no lo hará correctamente. Este tipo de sordera congénita es conocida como DFNB9.
Se han identificado más de 200 mutaciones en el gen OTOF que tienen como secuencia un déficit en la audición. En algunos casos se han identificado mutaciones que provocan que la sordera se potencie durante un episodio de fiebre o aumento de la temperatura corporal.
Muchas de estas mutaciones se han identificado en dominios C2, los cuales son capaces de unir calcio. La otoferlina tiene seis dominios de este tipo, que cuando son alterados pasan a unir calcio con menos afinidad o simplemente dejar de unirlo, lo que lleva a que la señal no se pueda transmitir y como consecuencia final a la sordera.
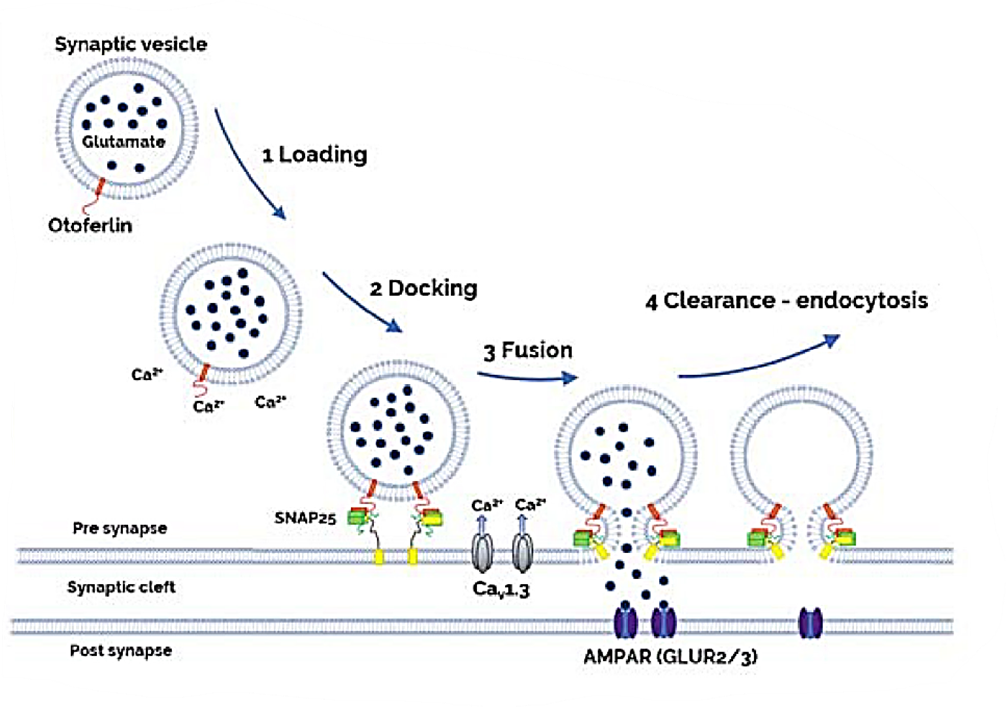
Front. Cell. Neurosci.
Resultados esperanzadores
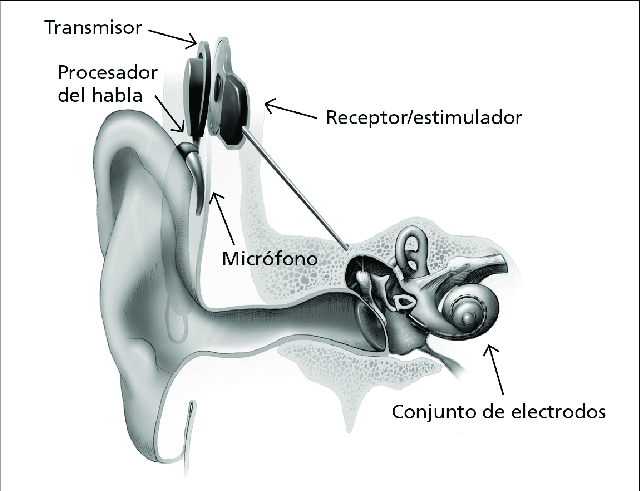
Hasta ahora la principal solución para tratar de revertir o minimizar esta sordera eran los implantes cocleares. Estos instrumentos sustituyen a la cóclea cuando esta no es funcional, encargándose de transformar una señal auditiva en una señal eléctrica que pueda ser procesada por nuestro sistema nervioso.
Pero las nuevas terapias génicas que han emergido tienen grandes ventajas respecto a este tipo de dispositivos y está previsto que los sustituyan en la mayoría de casos en el futuro.
Como hemos comentado, el objetivo de las terapias génicas es reestablecer el normal funcionamiento de la otoferlina, de tal forma que la transmisión de la señal eléctrica se produzca sin impedimento.
Dos terapias génicas se han desarrollado en los últimos tiempos, ambas basadas en la transferencia de una copia funcional del gen OTOF para que las células ciliadas del oído interno puedan producir otoferlina. Ambas terapias se han desarrollado utilizando un adenovirus como vector y en ambas la transferencia del gen se realiza en dos partes. Es decir, se divide el gen en dos debido a que su tamaño es demasiado grande como para entrar completo en un vector.
De esta forma se administra una copia funcional del gen OTOF a las células ciliadas del oído interno en dos partes transportadas por dos adenovirus. Ambos segmentos se unen en el interior de la célula para generar una copia funcional del gen. De esta forma la célula podrá utilizar este material genético y será posible restituir la producción de otoferlina. Además, los efectos off-target -efectos no deseados en otras células o tejidos- son mínimos, al estar esta copia controlada por un promotor específico de las células del oído interno.
La terapia AK-OTOF, desarrollada por Akouos -propiedad de la farmacéutica Lilly-, ha mostrado resultados positivos en un niño de 11 años con sordera congénita. Igualmente, se han publicado resultados positivos de la terapia AAV1-hOTOF, desarrollada por investigadores de la Universidad de Fudan (Shanghai).
Ambas terapias están todavía sin aprobar y se debe seguir evaluando la eficacia y seguridad a largo plazo, pero suponen un gran avance en la búsqueda de una terapia que permita restituir la audición.
Conclusión
Las terapias génicas son y serán de gran utilidad para el tratamiento de un gran número de enfermedades. Dentro de los avances que suponen estas terapias está la recuperación de la audición que ha sido ya efectivo en los últimos ensayos. Son todavía primeras aproximaciones pero este tipo de terapias serán seguro una realidad en la clínica en un futuro próximo.
¿Te apasionan las terapias génicas y la genética en general? Si necesitas formación en esta área, en genómica o biología celular tienes la oportunidad de formarte con el innovador Máster en Genética, Genómica y Biología Celular que ofrece la escuela superior STEM Future Education.
Artículo editado por Equipo de Microbacterium
Bibliografía
Akil O, Dyka F, Calvet C, Emptoz A, Lahlou G, Nouaille S, et al. Dual AAV-mediated gene therapy restores hearing in a DFNB9 mouse model. Proc Natl Acad Sci U S A. 2019 https://pubmed.ncbi.nlm.nih.gov/30782832/
Al-Moyed H, Cepeda AP, Jung S, Moser T, Kügler S, Reisinger E. A dual‐AAV approach restores fast exocytosis and partially rescues auditory function in deaf otoferlin knock‐out mice. EMBO Mol Med. 2019;11(1). Disponible en: https://pubmed.ncbi.nlm.nih.gov/30509897/
Azaiez H, Thorpe RK, Smith RJH. OTOF-Related Deafness. University of Washington, Seattle; 2021.
Da Rold C. Gene therapy allows a deaf child to hear for the first time. Nat Italy. 2024; https://www.nature.com/articles/d43978-024-00032-3
Eli Lilly and Company. Positive phase 1/2 clinical trial data for an investigational gene therapy for genetic hearing loss to be presented at the association for research in otolaryngology 2024 MidWinter meeting. https://investor.lilly.com/news-releases/news-release-details/positive-phase-12-clinical-trial-data-investigational-gene?_ga=2.121161160.1389196726.1708382327-250457422.1708382327
Hams N, Padmanarayana M, Qiu W, Johnson CP. Otoferlin is a multivalent calcium-sensitive scaffold linking SNAREs and calcium channels. Proc Natl Acad Sci U S A. 2017;114(30):8023–8. http://dx.doi.org/10.1073/pnas.1703240114
Jiang L, Wang D, He Y, Shu Y. Advances in gene therapy hold promise for treating hereditary hearing loss. Mol Ther. 2023;31(4):934–50. https://pubmed.ncbi.nlm.nih.gov/36755494/
Kaiser J. Gene therapies that let deaf children hear bring hope- and many questions. 2024. Science.org. https://www.science.org/content/article/gene-therapies-let-deaf-children-hear-bring-hope-and-many-questions
Leclère J-C, Dulon D. Otoferlin as a multirole Ca2+ signaling protein: from inner ear synapses to cancer pathways. Front Cell Neurosci. 2023;17. http://dx.doi.org/10.3389/fncel.2023.1197611
Lee CS, Bishop ES, Zhang R, Yu X, Farina EM, Yan S, et al. Adenovirus-mediated gene delivery: Potential applications for gene and cell-based therapies in the new era of personalized medicine. Genes Dis. 2017;4(2):43–63. http://dx.doi.org/10.1016/j.gendis.2017.04.001
Lv J, Wang H, Cheng X, Chen Y, Wang D, Zhang L, et al. AAV1-hOTOF gene therapy for autosomal recessive deafness 9: a single-arm trial. Lancet. 2024;http://dx.doi.org/10.1016/s0140-6736(23)02874-x
Sánchez-Vallejo MA. Una terapia génica devuelve la audición a un niño de 11 años con sordera congénita. Ediciones EL PAÍS S.L. 2024.https://elpais.com/ciencia/2024-01-23/una-terapia-genica-devuelve-la-audicion-a-un-nino-de-11-anos-con-sordera-congenita.html
Tolosa, A. La terapia génica abre vías terapéuticas para la pérdida auditiva. Genotipia. 2024. https://genotipia.com/genetica_medica_news/terapia-genica-perdida-auditiva/







