Hoy hablaremos de las neoplasias hematológicas, como el Mieloma Múltiple, y como errores en determinados procesos pueden acabar dando lugar al desarrollo de células malignas.
El envejecimiento y sus problemas derivados, como el cáncer, es uno de los principales problemas al que se enfrentan las sociedades modernas, ya que con la edad es más probable que ocurran fallos en los mecanismos que tiene nuestro organismo para evitar el desarrollo de células malignas.
La médula ósea en los adultos se encuentra en el interior de los huesos largos como el fémur o el esternón. Este tejido esponjoso representa el lugar donde viven las diversas células madre que darán lugar a las diferentes células sanguíneas como glóbulos rojos, macrófagos, plaquetas, linfocitos B o linfocitos T, etc, en un proceso llamado hematopoyesis. Por ello que la hematopoyesis ocurra correctamente, ya que de ello dependen el funcionamiento del sistema circulatorio y el sistema inmune.
Y es que vivimos en un mundo rodeados de microorganismos, algunos simplemente viven en el mismo mundo que nosotros sin causarnos ningún problema, otros son imprescindibles para el correcto funcionamiento de nuestro cuerpo y otros nos pueden llegar a causar enfermedades. Para evitar el desarrollo de microorganismos patógenos en nuestro organismo, tenemos un sistema inmune tan complejo como eficaz. Sin embargo, pueden darse ocasiones en las que las células encargadas de protegernos sean las causantes de severos problemas, como alergias, enfermedades autoinmunes o algunos tipos de cáncer.
Este es el caso del Mieloma Múltiple, una enfermedad provocada por células plasmáticas malignas. Estas células son linfocitos B maduros, que en una situación normal son las encargadas de producir anticuerpos que respondan de manera específica frente a los agentes extraños que entran en nuestro cuerpo.

Índice de contenido:
Generación de anticuerpos
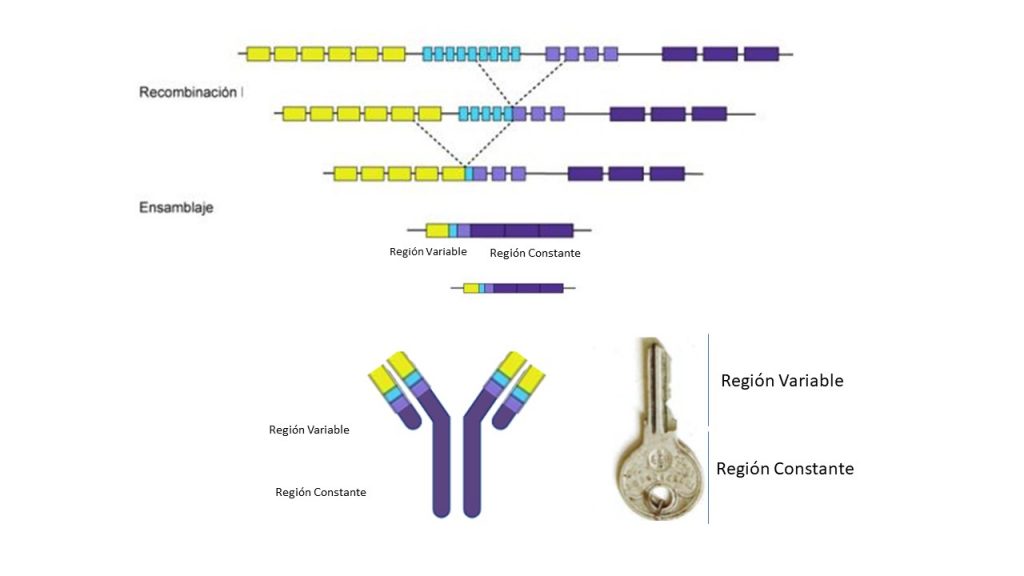
Los linfocitos B responden frente a los elementos que reconocen como extraños, los antígenos, generando unas proteínas llamadas anticuerpos. Cada anticuerpo reconoce un único antígeno, por lo que su unión es altamente específica. El resultado de esta unión puede llevar a la destrucción del antígeno o servir como una señal para que otros glóbulos blancos destruyan ese antígeno.
Teniendo en cuenta la gran variedad de microorganismos a la que estamos expuestos, debemos tener un repertorio de linfocitos B también muy variado y que permita la producción de distintos tipos de células plasmáticas, linfocitos B maduros encargados de la secreción de anticuerpos. El proceso por el que se genera tanta variabilidad implica un mecanismo muy complejo.
De este modo, el material genético de los linfocitos B se corta y reorganiza numerosas veces, de tal manera que, por azar, alguna combinación de genes será la adecuada para detectar y atacar a un determinado patógeno. Una vez se ha dado con la combinación necesaria, los linfocitos B se diferencian a células plasmáticas, que son las encargadas de producir y secretar los anticuerpos específicos.
Además, una vez se consigue la combinación adecuada para acabar con ese patógeno, la siguiente vez que entremos en contacto con sus antígenos, nuestra respuesta será más eficiente, ya que habremos desarrollado memoria inmunológica frente a esa amenaza.
camino para llegar a ser terapia» en la revista CONTRIBUCIONES CIENTÍFICAS Y TECNOLÓGICAS – VOL. 43 I Nº 2 I Pag. 7-20 (2018).
Este proceso es maravilloso y muy útil ya que nos permite tener infinitas combinaciones de genes y poder así generar linfocitos específicos contra cualquier patógeno. Sin embargo, el hecho de poseer un repertorio de linfocitos tan diverso implica un gran riesgo. Y es que, como hemos dicho, el material genético de los linfocitos B sufre muchas modificaciones durante la búsqueda de la combinación correcta que genere un linfocito específico contra un patógeno específico. Esto implica que durante este proceso la célula puede cometer errores dando lugar a mutaciones que pueden desencadenar la aparición de células cancerosas.
El desarrollo de células malignas
A pesar de todo esto, el desarrollo de células malignas no es tan sencilla, ya que nuestras células poseen mecanismos muy eficaces para reparar estos errores o eliminar las células que los poseen. Sin embargo, con el paso de los años estos mecanismos de reparación son cada vez más propensos a fallar. No obstante, para el desarrollo de un tumor no basta con una única mutación, sino que se requiere una sucesión de mutaciones que otorgue a las células malignas una alta capacidad para proliferar y sobrevivir.
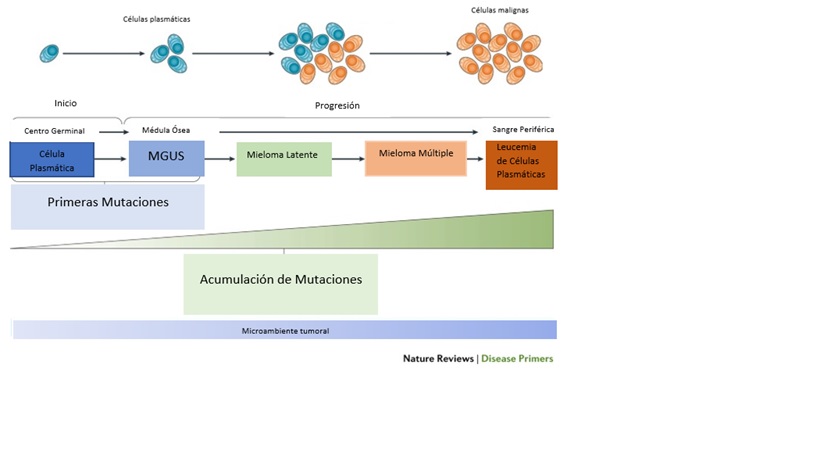
En el caso del Mieloma múltiple, las primeras mutaciones provocan la aparición de células plasmáticas aberrantes, que secretan grandes cantidades de un anticuerpo, llamada proteína monoclonal o proteína M. Este estadio se denomina Gammapatía Monoclonal de Significado Incierto, MGUS por sus siglas en inglés, y no genera ninguna sintomatología en el paciente con Mieloma múltiple, pero puede acabar progresando Mieloma múltiple. En algunos casos puede haber una fase intermedia denominada Mieloma latente del Mieloma múltiple, que tampoco causa síntomas.
Actualmente no están muy claras las causas que pueden desencadenar la aparición de síntomas a partir de estos dos estadios previos. Por ello es importante seguir investigando las diferencias entre los diferentes estadios para tratar de parar el desarrollo del Mieloma múltiple.
Mieloma múltiple
Teniendo en cuenta lo mencionado anteriormente, podemos definir el Mieloma Múltiple como una enfermedad en la que aparecen células plasmáticas malignas que se acumulan en la médula ósea secretando la proteína M, dando lugar a la aparición de los síntomas característicos de esta enfermedad: anemia, lesiones óseas, hipercalcemia y daño renal.
- La proliferación de células plasmáticas malignas en la médula ósea causa problemas para el correcto funcionamiento de la hematopoyesis, dando lugar a la anemia.
- Además, las células malignas son capaces de producir alteraciones en las células que les rodean, para su propio beneficio. Estas células forman el llamado microambiente celular, que en la médula ósea es el encargado de dar soporte a las células hematopoyéticas, aportando las señales necesarias para su correcto crecimiento y maduración. Además, este microambiente protege las células cancerosas de los diferentes tratamientos, siendo uno de los factores principales involucrados en la resistencia del tumor al tratamiento y de las posibles recaídas. Unos tipos celulares que viven en este microambiente medular son osteoblastos y osteoclastos, las células encargadas de crear y destruir el hueso, respectivamente. Las células malignas son capaces de activar los osteoclastos e inhibir los osteoblastos, provocando la destrucción del hueso. Esto da lugar a lesiones óseas e hipercalcemia, ya que se libera el calcio que contiene la estructura ósea.
- Por otro lado, el daño renal es causado por la excesiva producción de la proteína M que debe ser eliminada por el riñón. Esta situación se ve agravada por la deshidratación, la hipercalcemia y fármacos que comprometen el funcionamiento renal.
Mieloma múltiple en la sociedad
El Mieloma múltiple es una enfermedad relativamente rara, no obstante, es el segundo tipo de cáncer hematológico más frecuente, representando el 1% de las enfermedades neoplásicas y alrededor del 13% de los cánceres hematológicos. En España, se estima que se diagnostican unos 3000 casos de Mieloma Múltiple al año, con una media de edad de 72 años. Pese a que en los últimos años se ha avanzado mucho en el tratamiento de esta enfermedad, hoy en día continúa siendo incurable, ya que los tratamientos actuales, pese a alargar y mejorar mucho la calidad de vida de los pacientes, tienen una alta probabilidad de recaída.
Uno de los tratamientos punteros y más prometedores son las células CAR T, que están siendo utilizadas para el tratamiento de diferentes tipos de cáncer. Este es un tratamiento muy especializado en el que las los linfocitos T del propio paciente se modifican en el laboratorio para que ataquen específicamente a las células malignas. En el caso del Mieloma múltiple se ha aprobado este tipo de terapias para pacientes que han recaído tras haber sido tratados con otras terapias.
Sin embargo, gracias a los avances tecnológicos de los últimos años cada vez entendemos mejor los mecanismos que desencadenan esta enfermedad, así como los involucrados en la progresión de la enfermedad. Por tanto, cada día estamos más cerca de conseguir desarrollar nuevos tratamientos contra el Mieloma múltiple, que sean más eficaces que mejoren la calidad de vida de los pacientes.
Referencias
Abbas, A. K., Lichtman, A. H., & Pillai, S. (2007). Cellular and molecular immunology (6th ed.). Philadelphia: Saunders Elsevier.
Brigle K, Rogers B. Pathobiology and Diagnosis of Multiple Myeloma. Semin Oncol Nurs. 2017; 33(3): 225-36.
Hideshima T, Bergsagel PL, Kuehl WM, Anderson KC. Advances in biology of multiple myeloma: clinical applications. Blood. 2004; 104(3): 607-18.
Kumar SK, Rajkumar V, Kyle RA, van Duin M, Sonneveld P, Mateos MV, et al. Multiple myeloma. Nat Rev Dis Primers. 2017;3:17046.
Sklavenitis-Pistofidis R, Bustoros M, Ghobrial IM. Bone marrow niche in multiple myeloma and its precursor states. HemaSphere. 2019;3(S2):121-3.
Terpos E, Ntanasis-Stathopoulos I, Dimopoulos MA. Myeloma bone disease: from biology findings to treatment approaches. Blood. 2019;133(14):1534-9.





